��Ŀ����
����Ŀ��������һ����Ҫ�Ļ�����Ʒ�������������������Ϊһ�����ҹ�ҵ��չˮƽ��һ�ֱ�־��Ŀǰ����Ҫ���������ǡ��Ӵ��������йؽӴ�������Ӧ2SO2+O2 ![]() 2SO3 �� ��˵������ȷ���ǣ� ��
2SO3 �� ��˵������ȷ���ǣ� ��
A.�÷�ӦΪ���淴Ӧ������һ�������¶������������������ȫ��ת��Ϊ��������
B.�ﵽƽ���Ӧ��ֹͣ�ˣ��ʴ�ʱ�����淴Ӧ��������Ҿ�Ϊ��
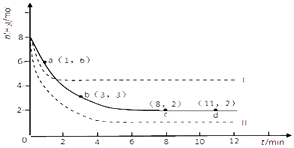
C.һ�������£���ij�ܱ������м���2molSO2��1molO2 �� ��ӷ�Ӧ��ʼ���ﵽƽ��Ĺ����У�����Ӧ���ʲ��ϼ�С���淴Ӧ���ʲ�������ijһʱ�̣������淴Ӧ�������
D.������������Ӧ������������ʱ��Ҫͬʱ���Ƿ�Ӧ���ܴﵽ���Ⱥͻ�ѧ��Ӧ���������������
���𰸡�B
���������⣺A�����淴Ӧ����һ�������²��ܽ��г��ķ�Ӧ������Ӧ���淴Ӧͬʱ���У��÷�ӦΪ���淴Ӧ������һ��������SO2��O2������ȫ��ת��ΪSO3 �� ��A��ȷ��B���ﵽƽ�������Ӧ���ʺ��淴Ӧ������ͬ���Ƕ�̬ƽ�⣬���ʲ���Ϊ0����B����
C��һ�������£���ij�ܱ������м���2 mol SO2��1mol O2 �� ��ӷ�Ӧ��ʼ��ƽ��Ĺ����У�����Ӧ���ʲ��ϼ�С���淴Ӧ���ʲ�������ijһʱ�̣������淴Ӧ������ȴﵽƽ�⣬��C��ȷ��
D����Ӧ�Ƿ��ȷ�Ӧ����Ϊ�˷�Ӧ������Ҫһ���¶ȣ������������ѹǿ�ڳ����£����������ת�����Ѿ���߸ı�ѹǿ��ת����Ӱ�첻��D��ȷ��
��ѡB��
A�����ݿ��淴Ӧ�����������жϣ�
B����ѧƽ���Ƕ�̬ƽ�⣬����Ӧ���ʺ��淴Ӧ������ͬ��
C������ƽ�⽨���Ĺ��̷�����
D���ϳ���Ҫ�����¶�ѹǿ��ƽ���Ӱ��;���Ч�森