题目内容
【题目】下列两组热化学方程式中,有关△H的比较正确的是( ) ①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H2
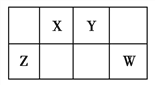
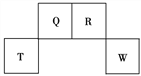
②NaOH(aq)+ ![]() H2SO4(浓)═
H2SO4(浓)═ ![]() Na2SO4(aq)+H2O(l)△H3
Na2SO4(aq)+H2O(l)△H3
NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H4 .
A.△H1>△H2;△H3>△H4
B.△H1>△H2;△H3<△H4
C.△H1=△H2;△H3<△H4
D.△H1<△H2;△H3<△H4
【答案】B
【解析】解:①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H2 , 两个反应都是放热反应,后者生成液态水,所以后者放出的热量大于前者,而放热反应△H小于0,放热越多,焓变值越小,故△H1>△H2;②NaOH(aq)+ ![]() H2SO4(浓)═
H2SO4(浓)═ ![]() Na2SO4(aq)+H2O(l);△H3、NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l);△H4 . 两个反应的实质是酸碱中和,都是放热反应,两个反应生成水的物质的量都是1mol,但是CH3COOH(aq)是弱电解质,电离过程吸收一部分热量,所以后者放出的热量小,所以△H3<△H4 , 故选B. △H为化学反应的焓变,放热反应的△H<0,吸热反应的△H>0;反应的热效应与反应物和生成物的状态有关,反应放出热量越大,焓变数值越小,据此进行解答.
Na2SO4(aq)+H2O(l);△H3、NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l);△H4 . 两个反应的实质是酸碱中和,都是放热反应,两个反应生成水的物质的量都是1mol,但是CH3COOH(aq)是弱电解质,电离过程吸收一部分热量,所以后者放出的热量小,所以△H3<△H4 , 故选B. △H为化学反应的焓变,放热反应的△H<0,吸热反应的△H>0;反应的热效应与反应物和生成物的状态有关,反应放出热量越大,焓变数值越小,据此进行解答.

 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案【题目】根据所学知识,完成下面题目:
(1)亚硝酰氯(ClNO)是有机合成中的重要试剂,可通过反应获得:NO(g)+Cl2(g)═2ClNO(g).①氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)△H1 K1
4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)△H2 K2
2NO(g)+Cl2(g)2ClNO(g)△H3 K3
则△H3=(用△H1和△H2表示),K3=(用K1和K2表示).
②NaOH溶液可以吸收氮的氧化物:NO2+NO+2NaOH=2NaNO2+H2O.室温下,用一定量的NaOH
溶液吸收NO、NO2混合气体,得到0.1mol/L的NaNO2溶液.已知HNO2的电离常数Ka=7.1×10﹣4 ,
那么室温下NO2﹣的水解常数Kh= , 0.1mol/L NaNO2溶液中从c(Na+ )、c(OH﹣ )、c(NO2﹣ )、c(HNO2)的大小顺序为 .
(2)在3.0L密闭容器中,通入0.10mol CH4和0.20molNO2 , 在一定温度下进行反应,CH4(g)+2NO2(g)CO2(g)+N2(g)+2H2O(g)△H<0,反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/min | 0 | 2 | 4 | 6 | 8 | 10 |
总压强p/100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
①由表中数据计算0~4min内v(NO2)= , 该温度下的平衡常数K=(不必带单位).
②在一恒容装置中,通入一定量CH4和NO2 , 测得在相同时间内,在不同温度下,NO2的转化率如图(横坐标为反应温度,纵坐标为NO2转化率/%):
则下列叙述正确的是 .
A.若温度维持在200℃更长时间,NO2的转化率将大于19%
B.反应速率:b点的v (逆)>e点的 v (逆)
C.平衡常数:c点=d点
D.提高b点时NO2的转化率和反应速率,可适当升温或增大c(CH4)
【题目】H2O2是常用的绿色氧化剂,H2S是还原剂,但H2S会对环境和人体健康带来极大危害。
I.H2S的除去,生物脱H2S的原理为:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4、4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O。
2Fe2(SO4)3+2H2O。
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_____。
(2)由图甲和图乙判断他用硫杆菌的最佳条件为_______。在最佳条件下,该反应的加热方式为_________,若反应温度过高,反应速率下降,其原因是__________。

II.为研究硫酸饮的量对过氧化氢分解速率的影响,某同学设计了如下一系列的实验。将表中所给的溶液分别加入A、B、C、D四个反应瓶中,收集产生的气体,在关数据如下:
实验溶液 | A/mL | B/mL | C/mL | D/mL |
0.4mol/LFe2(SO4)3溶液 | 0 | 1.0 | 2.0 | V1 |
30%H2O2溶液 | V2 | 20.0 | 20.0 | 20.0 |
H2O | 18.0 | 17.0 | V3 | 15.0 |
(1)实验过程中需记录的数据是___________。
(2)上表中的V2=_______,V3=_________。