��Ŀ����
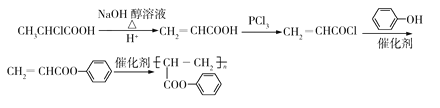
����Ŀ���л���F������ij����Ѫҩ���Ʊ�����ҵ����F��һ��·��ͼ���£�����H��FeCl3��Һ�ܷ�����ɫ��Ӧ����
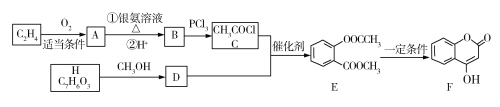
�ش��������⣺
��1��A��������______________��E�еĹ�������������_____________��
��2��B��C�ķ�Ӧ������_____________��F�ķ���ʽΪ_______________��
��3��H�Ľṹ��ʽΪ_________________��
��4��E��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ__________________________________��
��5��ͬʱ��������������D��ͬ���칹�干��________�֣�д���˴Ź���������5�������ʵĽṹ��ʽ____________��
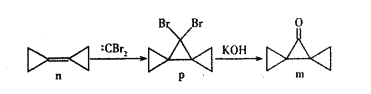
���Ƿ����廯����
������NaHCO3��Һ��Ӧ��������Na2CO3��Һ��Ӧ
��1 mol���������Ʒ�Ӧʱ���ɵõ�1 mol H2
��6����2�ȱ��ᡢ����Ϊԭ���Ʊ��۱�ϩ�ᱽ����(![]() )��д���ϳ�·��ͼ�����Լ���ѡ��_________________________________________________��
)��д���ϳ�·��ͼ�����Լ���ѡ��_________________________________________________��
���𰸡���ȩ ���� ȡ����Ӧ C9H6O3 ![]()
![]() +3NaOH��
+3NaOH��![]() + CH3COONa+CH3OH+H2O 4
+ CH3COONa+CH3OH+H2O 4 ![]()
��������
��1��~��4����A������֪������ȩ����ȩ������Ϊ���ᣬ������PCl3����ȡ����Ӧ����C����H��D��E��ת����ϵ��E��C�Ľṹ��ʽ����֪HΪ![]() ��DΪ
��DΪ![]() ��E�����к���2����������NaOH��Һ��Ӧ����
��E�����к���2����������NaOH��Һ��Ӧ����![]() ��CH3COONa��CH3OH��H2O��
��CH3COONa��CH3OH��H2O��
��5���ɢ�֪�����к��б������ɢ�֪�����к�����COOH�Ҳ������ǻ����ɢ�֪�����л����д��ǻ�����������ֻ��һ��ȡ����ʱ��ȡ����Ϊ��CHOHCOOH����������������ȡ����ʱ������ȡ�����ֱ�Ϊ��CH2OH����COOH������ȡ�����ڱ�����3��λ�ù�ϵ���ʹ���4��ͬ���칹�塣���к˴Ź���������5����������![]() ��
��
��6��2�ȱ����ȷ�����ȥ��Ӧ�õ���ϩ���ƣ��ữ����PCl3��Ӧ�õ�CH2=CHCOCl�����뱽�ӷ���ȡ����Ӧ��������Ӿ۷�Ӧ���ɡ�
��1����ϩ������������A��A�ܹ���������Һ��Ӧ���ɴ˿�֪AΪ��ȩ����E�Ľṹ��ʽ��֪E�еĹ�����Ϊ������
�ʴ�Ϊ����ȩ��������
��2����ȩ������������Һ��Ӧ���������ƣ��پ����ữ�������ᣬ��BΪ���ᣬ������PCl3������Ӧ����C����C�Ľṹ��֪�������е�-OH��Clȡ������C���䷴Ӧ����Ϊȡ����Ӧ����F�Ľṹ��ʽ��֪��F�ķ���ʽΪ��C9H6O3��
�ʴ�Ϊ��ȡ����Ӧ��C9H6O3��
��3����H��D��E��ת����ϵ��E��C�Ľṹ��ʽ����֪HΪ![]() ��
��
�ʴ�Ϊ��![]() ��
��
��4��E�к���2����������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ��![]() +3NaOH��
+3NaOH��![]() + CH3COONa+CH3OH+H2O��
+ CH3COONa+CH3OH+H2O��
�ʴ�Ϊ��![]() +3NaOH��
+3NaOH��![]() + CH3COONa+CH3OH+H2O��
+ CH3COONa+CH3OH+H2O��
��5����E�Ľṹ��H�Ľṹ��֪��D�Ľṹ��ʽΪ![]() ��
��
�ɢٿ�֪�����к��б�����
�ɢڿ�֪�����к�����COOH�Ҳ������ǻ���
�ɢۿ�֪�����л����д��ǻ�������л������ܲ����Ͷ�Ϊ5������ռ4�������Ͷȣ��Ȼ�ռ1�������Ͷȣ�����һ���ܹ����Ʒ�Ӧ����H2�Ĺ�����Ϊ�ǻ�����
������������л���Ϊ��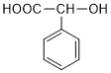 (1��)��
(1��)��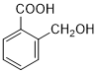 (�ڼ�Թ�3��)���ʹ���4�ֽṹ�����к˴Ź���������5��壬����ͬ��ѧ��������ԭ����5�֣�������Ϊ��
(�ڼ�Թ�3��)���ʹ���4�ֽṹ�����к˴Ź���������5��壬����ͬ��ѧ��������ԭ����5�֣�������Ϊ��![]() ��
��
�ʴ�Ϊ��4��![]() ��
��
��6��![]() �ĵ���Ϊ��
�ĵ���Ϊ��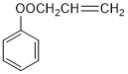 ����
���� �ͱ���Ϊԭ�ϣ����Ⱥϳ�
�ͱ���Ϊԭ�ϣ����Ⱥϳ� ��Ȼ��ͨ���Ӿ۷�Ӧ���ɾ۱�ϩ�ᱽ��������ϳ�·��ͼΪ��
��Ȼ��ͨ���Ӿ۷�Ӧ���ɾ۱�ϩ�ᱽ��������ϳ�·��ͼΪ��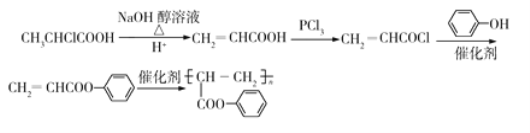 ��
��
�ʴ�Ϊ��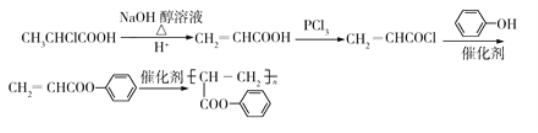 ��
��

 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д� ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д�����Ŀ���������ȣ�ClNO�����л��ϳ��е���Ҫ�Լ����������ȿ���NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO(g)+Cl2(g)![]() 2ClNO(g)��
2ClNO(g)��
��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
��4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g��+Cl2(g) K1
2NaNO3(s)+2NO(g��+Cl2(g) K1
��2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K2
NaNO3(s)+ClNO(g) K2
��2NO(g)+Cl2(g)![]() 2ClNO(g) K3
2ClNO(g) K3
��K1��K2��K3֮��Ĺ�ϵΪK3=____________��
��2��T��ʱ��2NO(g)+Cl2(g)![]() 2ClNO(g)������Ӧ���ʱ���ʽΪ����=kcn(ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
2ClNO(g)������Ӧ���ʱ���ʽΪ����=kcn(ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
��� | c(ClNO)/mol��L��1 | ��/mol��L��1�� s��1 |
�� | 0.30 | 3.6��10��8 |
�� | 0.60 | 1.44��10��7 |
�� | 0.90 | 3.24��10��7 |
n=__________��k=___________��ע����λ����
��3����2 L�ĺ����ܱ������г���4 mol NO(g)��2molCl2(g)���ڲ�ͬ�¶��²��c(ClNO)��ʱ��Ĺ�ϵ��ͼI��

�� �¶�ΪT1ʱ������Ϊ�÷�Ӧ�ﵽƽ��ı�־����__________��
a.����������ֲ��� b.����ѹǿ���ֲ��� c.ƽ�ⳣ��K���ֲ���
d.������ɫ���ֲ��� e.��(ClNO)=��(NO) f.NO��ClNO�����ʵ�����ֵ���ֲ���
�� ��Ӧ��ʼ��10minʱ��Cl2��ƽ����Ӧ������(Cl2)=_______________��
�� �¶�ΪT2ʱ��10 minʱ��Ӧ�Ѿ��ﵽƽ�⣬�÷�Ӧ��ƽ�ⳣ��K=____________��
��4��һ���������ں��º��ݵ��ܱ������а�һ����������NO(g)��Cl2(g)��ƽ��ʱClNO�������������![]() �ı仯��ͼII����A��B��C����״̬�У�NO��ת������С����____�㣬��
�ı仯��ͼII����A��B��C����״̬�У�NO��ת������С����____�㣬��![]() ʱ���ﵽƽ��״̬ʱClNO�����������������D��E��F�����е�_____�㡣
ʱ���ﵽƽ��״̬ʱClNO�����������������D��E��F�����е�_____�㡣