题目内容
【题目】下列说法错误的是
A.O2-、F-、Na+、Mg2+半径依次减小
B.O2和O3是氧元素的同素异形体
C.同一元素的不同核素化学性质几乎完全相同
D.同主族元素含氧酸的酸性随核电荷数的增加而减弱
【答案】D
【解析】
A.具有相同排布的离子,原子序数大的离子半径小,则O2﹣、F﹣、Na+、Mg2+半径依次减小,故A正确;
B.O2和O3是氧元素形成的两种不同单质,两者互为同素异形体,故B正确;
C.同一元素的不同核素,有相同的核外电子排布,所以化学性质相同,故C正确;
D.同主族自上而下非金属性减弱,最高价含氧酸的酸性减弱,非最高价含氧酸则不一定,故D错误;
故选:D。

【题目】卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子的易溶盐。以卤块为原料可制得轻质氧化镁,工艺流程如图:
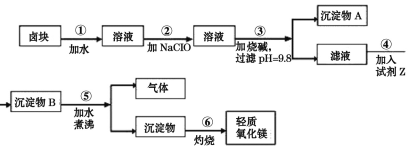
已知:(1)Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(2)原料价格表
物质 | 价格/(元·吨-1) |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
(3)生成氢氧化物沉淀的PH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
回答下列问题:
(1)某课外兴趣小组设计实验证明卤块中含有Fe3+为:取少许样品加水溶解,____,则说明卤块中含Fe3+。
(2)工业上冶炼镁常用的方法的化学方程式为____。
(3)步骤②加入NaClO而不用H2O2的原因是____,步骤②反应后产生少量红褐色沉淀,该反应中氧化剂与还原剂的比例为____。
(4)沉淀A的主要成分为____;步骤④加入的物质为____。
(5)步骤⑤发生的反应的化学方程式为____。
(6)步骤⑥如在实验室进行,应选用在____(填仪器名称)中灼烧。