题目内容
1.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 常温下,1L0.1mol•L-1氢氟酸溶液中含有的H+离子数为0.1NA | |
| B. | 密闭容器中,2molSO2与4molO2充分反应转移的电子数为4NA | |
| C. | 25℃时,pH=13的Na2CO3溶液中含有的OH-两种数为NA | |
| D. | 常温下,1L1mol•L-1NaOH溶液中含有的阳离子总数大于NA |
分析 A.氢氟酸是弱酸,部分电离;
B.可逆反应不能进行到底;
C.溶液体积不明确;
D.阳离子有氢离子和钠离子.
解答 解:A.氢氟酸是弱酸,部分电离,1L0.1mol•L-1氢氟酸溶液中含有的H+离子数小于0.1NA,故A错误;
B.可逆反应不能进行到底,转移的电子数小于4NA,故B错误;
C.溶液体积不明确,无法计算OH-的数目,故C错误;
D.阳离子有氢离子和钠离子,钠离子总数为NA,阳离子总数大于NA,故D正确.
故选D.
点评 本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.

练习册系列答案
相关题目
4.下列有关实验的叙述正确的是( )
| A. | 实验室用浓溴水与苯在Fe粉催化下制溴苯 | |
| B. | 欲检验CH2=CHCHO中的碳碳双键,应向其中先加入足量的新制银氨溶液,水浴加热,待出现银镜后,再加入适量的溴水,若溴水褪色,即可验证 | |
| C. | 实验室制备乙酸乙酯时,向试管中加入试剂的顺序为:乙醇、浓硫酸、冰醋酸 | |
| D. | 将CH3CH2Br与NaOH溶液共热后,向其中加入AgNO3溶液,若产生沉淀,即可证明CH3CH2Br中含有溴元素 |
5.除去下列物质中含有的少量杂质(括号内为杂质)方法正确的是( )
| A. | C2H6(C2H4),用镍做催化剂共热. | |
| B. | C2H4(SO2),通过盛氯水溶液洗气瓶,再用碱石灰干燥 | |
| C. | 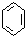 ( (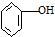 )加入过量浓溴水,先过滤;再分液 )加入过量浓溴水,先过滤;再分液 | |
| D. | C2H5Br(C2H5OH)先用大量水洗涤,然后分液 |
2.下列反应属于取代反应的是( )
| A. | 在光照条件下甲烷和氯气生成一氯甲烷的反应 | |
| B. | 乙醇和酸性高锰酸钾溶液的反应 | |
| C. | 乙烯和溴的四氯化碳溶液的反应 | |
| D. | 镍作催化剂、加热的条件下苯和氢气的反应 |
9.下列各组混合物,不论三者以什么比例混合,只要总质量一定,完全燃烧时生成CO2的质量也一定的是( )
| A. | 乙炔、苯、丙炔 | B. | 乙醇、甲酸、乙酸 | ||
| C. | 甲醛、乙酸、葡萄糖 | D. | 丙烯、乙烯、2-戊烯 |
6.萘(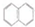 )一氯代物的同分异构体有( )
)一氯代物的同分异构体有( )
 )一氯代物的同分异构体有( )
)一氯代物的同分异构体有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
10.下列说法正确的是( )
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 | |
| B. | 100mL 2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化是一个放热的反应,所以升高温度,反应的速率减慢 | |
| D. | 在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 |
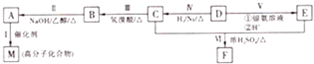
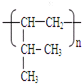
 :
: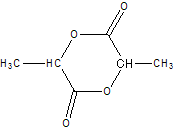 、
、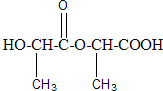 .
.