题目内容
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是
| A.X的气态氢化物比Y的稳定 |
| B.Z的非金属性比Y的强 |
| C.W的最高价氧化物对应水化物的酸性比Z的强 |
| D.X与Y形成的化合物都能与水反应 |
C
解析试题分析:根据Y原子的最外层电子是内层电子数的3倍可得Y为氧,则X为N,Z为S,W为Cl;同周期从左向右气态氢化物的稳定性逐渐增强,最高价氧化物对应水化物的酸性逐渐增强,故A错误,C正确;同主族从上到下非金属性逐渐减弱,故B错误;N和O形成的化合物NO不能和水反应,故D错误;故选C。
考点:元素的推断、元素周期律的应用、元素周期律。

练习册系列答案
相关题目
据最新报道,放射性同位素钬 Ho可有效地治疗肝癌。该同位素原子的质量数与核电荷数之差为
Ho可有效地治疗肝癌。该同位素原子的质量数与核电荷数之差为
| A.32 | B.67 | C.99 | D.166 |
已知下列元素原子的最外层电子排布式,其中不能表示该元素一定为主族元素的是
| A.3s23p3 | B.4s2 | C.4s24p1 | D.3s23p5 |
下列各组物质的性质由强到弱的顺序排列正确的是
| A.酸性:HClO4>H3PO4>H2SO4 | B.氢化物稳定性:H2S>HF>H2O |
| C.碱性:NaOH>Al(OH)3>Mg(OH)2 | D.氧化性:F2 > Cl2 > Br2 > I2 |
若aAn+与bB2-两种离子的核外电子层结构相同,则a的数值为( )
| A.b+n+2 | B.b+n-2 | C.b-n-2 | D.b-n+2 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )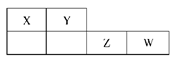
| A.氢化物稳定性:X>Y |
| B.最高价氧化物对应的水化物的酸性:W>Y |
| C.4种元素的单质中,W单质的熔、沸点最高 |
| D.干燥的W单质具有漂白性 |