题目内容
【题目】将O2和NH3的混合气体448mL通过加热的三氧化二铬,充分反应后,再通过足量的水,最终收集到44.8mL气体。原混合气体中O2的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)( )
A.231.5mLB.313.6 mLC.287.5mLD.368.8
【答案】B
【解析】
混合气体的总物质的量为n= ![]() =0.02mol,而剩余的氧气的物质的量为n=
=0.02mol,而剩余的氧气的物质的量为n= ![]() =0.002mol,故反应掉的O2和NH3的物质的量之和为0.02mol-0.002mol=0.018mol,设氧气的物质的量为xmol,氨气的物质的量为ymol,则有x+y=0.018mol ①;由于NH3反应后最终变为+5价、O2反应后变为-2价,根据反应得失电子数守恒可得:4x=8y ②;解①②可知:x=0.012mol,y=0.006mol故氧气的总量为0.012mol+0.002mol=0.014mol,在标况下的体积V=nVm=0.014mol×22.4L/mol=313.6mL,故选B。
=0.002mol,故反应掉的O2和NH3的物质的量之和为0.02mol-0.002mol=0.018mol,设氧气的物质的量为xmol,氨气的物质的量为ymol,则有x+y=0.018mol ①;由于NH3反应后最终变为+5价、O2反应后变为-2价,根据反应得失电子数守恒可得:4x=8y ②;解①②可知:x=0.012mol,y=0.006mol故氧气的总量为0.012mol+0.002mol=0.014mol,在标况下的体积V=nVm=0.014mol×22.4L/mol=313.6mL,故选B。

 科学实验活动册系列答案
科学实验活动册系列答案【题目】(1)为了检验和除去表中的各种杂质(括号里的为杂质),请从①中选出适当的检验试剂,从②中选出适当的除杂试剂,将所选的答案用字母填入相应的空格内。
物质 | 检验试剂 | 除杂试剂 |
(Ⅰ)甲烷(乙烯) | ____ | ____ |
(Ⅱ)酒精(水) | ____ | ____ |
①检验的试剂:a.无水硫酸铜b.酸性高锰酸钾溶液c.水d.氢氧化钠溶液
②除杂试剂:a.无水硫酸铜b.乙酸c.新制的生石灰d.溴水
(2)如图所示,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3 mL浓硫酸,再加入2 mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5 min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
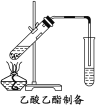
试回答:在右试管中通常加入__________溶液,实验生成的乙酸乙酯,其密度比水小,是有特殊香味的液体。分离右试管中所得乙酸乙酯的操作为__________(只填名称)。反应中加入浓硫酸的作用是__________。