题目内容
17.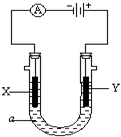 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为2H++2e-=H2↑.在X极附近观察到的现象是放出气体,溶液变红.
②Y电极上的电极反应式为2Cl--2e-=Cl2↑,检验该电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是纯铜,电极反应式是Cu2++2e-=Cu.
(3)此装置若是在某金属上电镀铜,则①X电极的材料是镀件,②Y电极的材料是纯铜,电解液a选用硫酸铜溶液.
分析 (1)电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子,氯气能使湿润的碘化钾淀粉试纸变蓝;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阴极上铜离子放电;
(3)此装置若是在某金属上电镀铜,则阴极为镀件,阳极为镀层金属,电解液为含镀层金属离子的盐溶液.
解答 解:(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,故答案为:2H++2e-=H2↑;放出气体,溶液变红;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,氯气能使湿润的碘化钾淀粉试纸变蓝,可以用于氯气的检验,
故答案为:2Cl--2e-=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色;
(2)电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu2++2e-=Cu,故答案为:纯铜; Cu2++2e-=Cu;
(3)此装置若是在某金属上电镀铜,则①X电极为阴极,材料是镀件,②Y电极为阳极,材料是纯铜,电解液a选用硫酸铜溶液,钴答案为:镀件,纯铜,硫酸铜.
点评 本题考查学生电解池的工作原理知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
12.下列各组离子能大量共存且溶液颜色为无色的是( )
| A. | Na+、MnO4-、K+、NO3-SO32- | B. | Na+、S2-、SO32-、H+、NO3- | ||
| C. | Na+、S2-、OH-、K+、Cl- | D. | HCO3-、H+、Na+、Ca2+ SO32- |
2.下列说法正确的是( )
| A. | 胶体区别于其他分散系的本质依据是具有丁达尔效应 | |
| B. | 通电时,溶液中的溶质粒子分别向两极移动,胶体粒子也一定会向某一极移动 | |
| C. | 纳米材料粒子直径一般在10-9m与10-7m之间,因此纳米材料属于胶体 | |
| D. | 在江河入海处容易形成沙洲与胶体的聚沉有关 |
9.碱性电池具有容量大,放电电流大的特点,因而得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn+2MnO2+2H2O═Zn(OH)2+2MnOOH,下列说法错误的是( )
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过0.2mol 电子,锌的质量理论上减少6.5g |
7.为了同时除去混在CO2气体中的杂质HCl和SO2,应选用的试剂是( )
| A. | NaOH溶液 | B. | 饱和NaHCO3溶液 | C. | Na2CO3溶液 | D. | CaO固体粉末 |
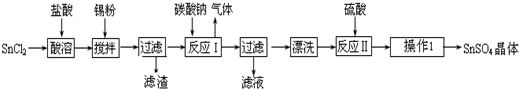
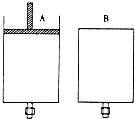 有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两只容器中分别充入等量的体积比为2:1的SO2与O2的混合气体,并使A和B容积相等(如图).在保持400℃的条件下使之发生如下反应:
有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两只容器中分别充入等量的体积比为2:1的SO2与O2的混合气体,并使A和B容积相等(如图).在保持400℃的条件下使之发生如下反应: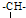 和一个-Cl,它的可能结构有四种,请写出这四种可能的结构简式:
和一个-Cl,它的可能结构有四种,请写出这四种可能的结构简式: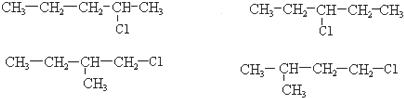 .
.