题目内容
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中该溶质的pC=-lg1×10-3=3。已知H2CO3溶液中存在的化学平衡为:CO2+H2O![]() H2CO3
H2CO3![]() H+ +HCO3—;HCO3—
H+ +HCO3—;HCO3—![]() H++CO32—。如图为H2CO3溶液的pC-pH图。请回答下列问题:
H++CO32—。如图为H2CO3溶液的pC-pH图。请回答下列问题:

(1)在pH=0~4时,H2CO3溶液中主要存在的离子为: ;在pH=12时,H2CO3溶液中主要存在的含碳阴离子为: ;
(2)pH<5时,溶液中H2CO3的pC值总是约等于3的原因是 ;
(3)一定浓度的NaHCO3和Na2CO3混合溶液是一种“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化不大,其原因是
(8分)(1)H+、HCO3—(2分) CO32—、HCO3—(2分)
(2)(2分)CO2本身在水中的溶解度小,加之酸性增强(或H+浓度增大),上述电离平衡向左移动放出CO2
(3)(2分)在该溶液中加入少量的酸,H+与CO32—结合生成HCO3—(或使平衡:
HCO3— ![]() H++CO32—向左移动,,结果溶液中H+浓度增加得很少;若在溶液中加入少量的碱,OH—与HCO3—结合生成CO32—(或使平衡HCO3—
H++CO32—向左移动,,结果溶液中H+浓度增加得很少;若在溶液中加入少量的碱,OH—与HCO3—结合生成CO32—(或使平衡HCO3— ![]() H++CO32—向右移动,,结果溶液中的OH—浓度也增加不大。
H++CO32—向右移动,,结果溶液中的OH—浓度也增加不大。

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol?L-1,则该溶液中溶质的pC=3.下列表达正确的是( )
| A、某温度下任何电解质的水溶液中,pC(H+)+pC(OH-)=14 | B、0.01mol/L的CaCl2溶液中逐渐滴加纯碱溶液,滴加过程中pC(Ca2+)逐渐减小 | C、用0.01mol/L的盐酸滴定某浓度的NaOH溶液,滴定过程中pC(H+)逐渐增大 | D、某温度下,AB难溶性离子化合物的Ksp=1.0×10-10,其饱和溶液中pC(A+)+pC(B-)=10 |
 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡: 此条件下,该反应达到化学平衡时,氮气的浓度为
此条件下,该反应达到化学平衡时,氮气的浓度为
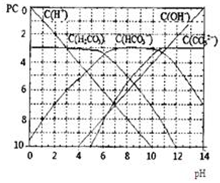 pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中溶质的pC=-lg1×10-3=3.图为H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC-pH图.请回答下列问题:
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中溶质的pC=-lg1×10-3=3.图为H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC-pH图.请回答下列问题: