题目内容
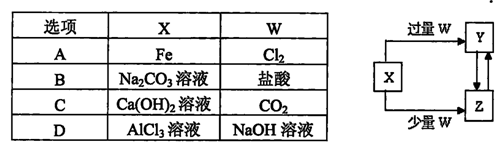
下列物质的转化在给定条件下能实现的是
①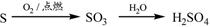
②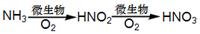
③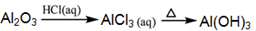
④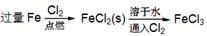
⑤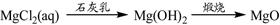
| A.②③⑤ | B.①④⑤ | C.③④⑤ | D.①③⑤ |
A
解析试题分析:①硫燃烧得到二氧化硫气体,二氧化硫催化氧化得到三氧化硫,三氧化硫溶于水得到硫酸;④铁是变价金属,遇到强氧化剂,如氯气生成氯化铁。
考点:考查物质的化学性质及相互转换关系。

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
HArF是第一个被发现的氩化合物,其分子的比例模型如图所示,在HArF中氟为-l价,氩为0价,其水溶液显强酸性,酸性与盐酸相当。下列有关说法错误的是( )
| A.稀有气体在一定条件下也可发生化学反应 |
| B.HAlF为极性分子 |
| C.ArF-具有较强的氧化性 |
| D.向HArF溶液中加入NaOH,反应的离子方程式为:H++OH-=H2O |
用图中所示的装置进行实验,实验现象与预测不一致的是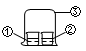
| | ①中的物质 | ②中的物质 | 预测现象 |
| A | 浓氨水 | FeCl3溶液 | ②中有红褐色沉淀 |
| B | 浓氨水 | 浓盐酸 | ③中有白烟 |
| C | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
| D | 饱和亚硫酸 | 蓝色石蕊试液 | ②中溶液先变红色又褪色 |
下述实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 取两只试管,分别加入4 mL 0.01 mol/L KMnO4酸性溶液,然后向一只试管中加入0.1 mol/L H2C2O4溶液 2 mL,向另一只试管中加入0.1 mol/L H2C2O4溶液 4 mL,记录褪色时间 | 证明草酸浓度越大反应速率越快 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向1mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下,溶解度Mg(OH)2 >Fe(OH)3 |
| D | 测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性S>C |
下列实验中,依据实验操作及现象,得出的结论正确的是( )
| | 操作 | 现象 | 结论 |
| A. | 用食醋浸泡水垢。[水垢成分: CaCO 3与Mg(OH)2] | 水垢溶解,有无色气泡 | 碱性:CH3COONa>Na2CO3 |
| B. | 浓硫酸与氯化钠固体微热 | 产生刺激性气味气体 | 酸性:H2SO4>HCl |
| C. | 向FeCl2溶液中通入过量Cl2 | 溶液由浅绿色变成黄色 | 还原性: > >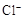 |
| D. | 向盛有1mL 0.1mol/LNaCl 溶液的试管中滴加2~4滴 0.1mol/LAgNO3溶液,后继续 滴加1mL 0.1mol/LKI溶液。 | 先出现白色沉淀,后变 成黄色沉淀 | 溶解度:AgI>AgCl |
下列实验现象可用同一原理解释的是
| A.品红溶液中分别通入SO2和Cl2,品红均褪色 |
| B.溴水分别滴入植物油和裂化汽油中,溴水均褪色 |
| C.鸡蛋白溶液中分别加入NaCl溶液和HgCl2溶液,均有固体析出 |
| D.分别加热盛有NH4Cl和单质碘的试管,管口均有固体凝结 |
S、N、Cl都是重要的非金属元素,下列说法正确是
| A.98%的浓硫酸用等体积的水稀释后,硫酸的质量分数为49% |
| B.SO32-、ClO-、NO3-三种离子在溶液中因发生氧化还原反应而不能大量共存 |
| C.浓硫酸、硝酸具有强氧化性,浓硝酸和浓盐酸易分解具有不稳定性 |
| D.标况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA个(NA为阿伏加德罗常数) |
类比推理是重要的学科思想,下列根据已知进行推理正确的是
| 选项 | 已知 | 类比推理 |
| A | Na与O2共热生成Na2O2 | H2与O2共热生成H2O2 |
| B | S、Se属于VIA族元素 | Se的氧化物类似S有SeO2、SeO3 |
| C | 常温下,浓硝酸使铁钝化 | 浓硝酸与铜不反应 |
| D | NaOH溶液能溶解Al(OH)3 | 过量NH3·H2O缓慢溶解Al(OH)3 |