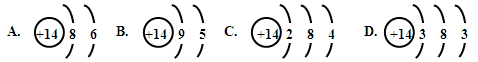题目内容
元素周期表中,划分周期的依据是
| A.元素的核电荷数 | B.元素原子的电子层数 |
| C.元素的化合价 | D.元素原子的最外层电子数 |
B
解析试题分析:元素周期律是依据元素原子的电子层排布规律进行排列的,因此答案选B
考点:考查元素周期律的相关知识点

练习册系列答案
相关题目
下列说法正确的是( )
| A.酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化的原因 |
| B.CH4、NH3、PH3的热稳定性逐渐增强 |
| C.因为酸性:HC1>HF,所以非金属性:Cl>F |
| D.钠原子在反应中失去的电子比铝原子少,故钠的金属性比铝弱 |
某元素原子的最外层有1个电子,则该元素不可能是
| A.IA族元素 | B.金属元素 | C.非金属元素 | D.惰性元素 |
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是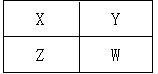
| A.非金属性:Z<X<Y |
| B.W的原子序数可能是Y的原子序数的2倍 |
| C.气态氢化物稳定性:Y<W |
| D.四种元素中不可能有金属元素 |
关于元素周期表的说法正确的是( )
| A.元素周期表有8个主族 | B.元素周期表有7个周期 |
| C.短周期是指第一、二周期 | D.IA族的元素全部是金属元素 |
根据表中信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
下列元素的最高价氧化物对应的水化物酸性最强的是
| A.第3周期有7个价电子的元素 |
| B.价电子排布式为3s23p2的元素 |
| C.原子的L电子层p轨道只填了2个电子的元素 |
| D.3p轨道电子半充满的元素 |