题目内容
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)含500mL 0.8 mol/L 的Al2(SO4)3中所含的SO![]() 的物质的量是___________。
的物质的量是___________。
(2)标准状况下,___________ L NH3所含氢原子数与0.2molH3PO4所含氢原子数相等。
(3)将20ml物质的量浓度为6mol/L的MgSO4加水稀释成100ml溶液,所得稀硫酸的物质的量浓度是_____________。
(4)a个X原子的总质量为bg,则X的相对原子质量可以表示为_______________。
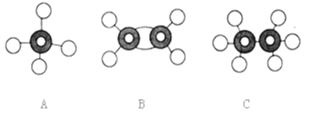
(5)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为__________,质量之比为__________。
(6)等质量的 SO2 和 SO3 物质的量之比是____________,氧原子数之比为____________。
(7)25.4 g某二价金属A的氯化物中含有0.4mol Cl-,则A的摩尔质量为____________。
【答案】1.2 mol 4.48 1.2mol/L ![]() 1:1 4:11 5:4 5:6 56g/mol
1:1 4:11 5:4 5:6 56g/mol
【解析】
根据物质的量公式及阿伏伽德罗定律和推论解答。
(1).含500mL 0.8 mol/L 的Al2(SO4)3中所含的SO![]() 的物质的量=0.5L×0.8mol/L×3=1.2mol,故答案为:1.2mol;
的物质的量=0.5L×0.8mol/L×3=1.2mol,故答案为:1.2mol;
(2).标准状况下,0.2molH3PO4所含氢原子数为0.6mol,要使 NH3所含氢原子数与之相等,则NH3的物质的量为0.2mol,NH3在标准状况下的体积为0.2mol×22.4L/mol=4.48L,故答案为:4.48;
(3).根据稀释时溶质的物质的量不变,即c1v1=c2v2,所以20ml×10-3×6mol/L=c×100ml×10-3,c=1.2mol/L,故答案为:1.2mol/L;
(4).a个X原子的物质的量为:![]() ,则摩尔质量为:
,则摩尔质量为: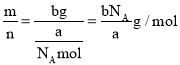 ,故答案为:
,故答案为:![]() ;
;
(5).根据阿伏伽德罗推论有,同温同压,体积之比等于物质的量之比,质量之比等于摩尔质量之比,故答案为:1:1;4:11;
(6).由公式![]() 可知,等质量的 SO2 和 SO3 物质的量之比等于摩尔质量的反比等于5:4,氧原子数之比为5:6,故答案为:5:4;5:6;
可知,等质量的 SO2 和 SO3 物质的量之比等于摩尔质量的反比等于5:4,氧原子数之比为5:6,故答案为:5:4;5:6;
(7).二价金属A的氯化物化学式为ACl2,,含有0.4mol Cl-,则A的物质的量为0.2mol,现A的氯化物质量为25.4g,则A的摩尔质量为56g/mol,故答案为:56g/mol。

【题目】(15分)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为____________。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) ===H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(4)Bodensteins研究了下列反应:2HI(g)![]() H2(g) + I2(g)
H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:___________。
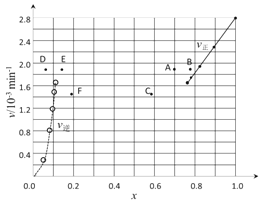
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=________min-1
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2/span>)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_________________(填字母)