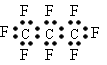
题目内容
下列现象能用键能大小解释的是
| A.稀有气体一般很难发生化学反应 | B.常温常压下,溴呈液态 |
| C.氮气的化学性质比氧气稳定 | D.硝酸容易挥发,而硫酸很难挥发 |
C
解析试题分析:A项中主要是原子最外层达到了稳定结构;B项是由于分子间作用力较大才使溴变了为液态;C是正确的;D是由于硝酸中存在分子内氢键使得其沸点比较低,不是键能的原因;
考点:考查键能和物质稳定性和物理性质的关系

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
下列说法不正确的是
①非金属元素构成的单质中一定存在共价键;②非金属之间形成的化合物一定是共价化合物;③非金属的气态氢化物中一定存在极性共价键;④离子化合物中一定含有离子键;⑤金属元素和非金属元素形成的化合物一定是离子化合物;⑥在一种化合物中只能存在一种类型的化学键;⑦含共价键的化合物不一定是共价化合物;⑧含离子键的化合物一定是离子化合物;⑨氯化钠和HCl溶于水都发生电离,克服粒子间作用力的类型相同
| A.③④⑦⑧ | B.①③④⑦⑧ | C.①②⑤⑥⑨ | D.①④⑦⑨ |
用价层电子对互斥理论预测H2S和CH2O分子的立体结构,两个结论都正确的是
| A.直线形;三角锥形 | B.V形;三角锥形 |
| C.直线形;平面三角形 | D.V形;平面三角形 |
现有如下各说法:( )
①在水分子中氢、氧原子间以共价键相结合;
②活泼金属和活泼非金属化合时一般形成离子键;
③非金属元素间形成的化合物一定是共价化合物;
④根据电离方程式HCl=H++Cl-,判断HCl分子里存在离子键;
⑤冰的密度比水的密度小,这与氢键有关;
上述各种说法正确的是
| A.①②⑤ | B.①②④⑤ | C.①②③④⑤ | D.①③④⑤ |
下列物质中,既含有离子键又含有极性共价键的是( )
| A.Na2O2 | B.MgCl2 | C.HCl | D.KOH |
下列各组分子中,都由极性键构成的极性分子的一组是
| A.H2O和NH3 | B.CCl4和H2S | C.C2H2和CO2 | D.H2O2和CS2 |
下列有关作用力的说法正确的是( )
| A.金属键、离子键、分子间作用力都没有方向性和饱和性 |
| B.键能、金属的原子化热、晶格能分别可以衡量氢键、金属键、离子键的强弱 |
| C.离子键、金属键、氢键、范德华力本质上都是静电作用 |
| D.乙酸、丙醇、丙酮的沸点都比丁烷高是因为前三者分子间都存在氢键 |
下列说法一定正确的是
| A.其水溶液导电的一定是离子化合物 |
| B.熔融态导电的一定是离子化合物 |
| C.固态导电的一定是金属单质 |
| D.固态不导电但熔融态导电的一定是离子化合物 |