题目内容
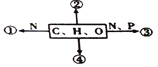
【题目】Ⅰ.尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)写出工业上以NH3、CO2为原料合成尿素的热化学方程式:_________________________
(2)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:

已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________步反应决定,总反应进行到_________min时到达平衡。
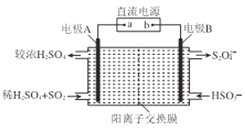
(3)电解尿素[CO(NH2)2]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为________________________________。
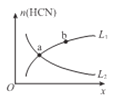
Ⅱ.用焦炭还原NO2的反应为:2NO2(g)+2C(s )![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
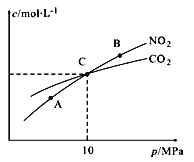
①A、B两点的浓度平衡常数关系:Kc(A)_______Kc(B) (填 “﹥”、“<”或“﹦”)。
②计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
【答案】 2NH3(g)+CO2(g)![]() H2O(g)+CO(NH2)2 (s) ΔH=-134kJ/mol 2 55 CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O = 2 MPa
H2O(g)+CO(NH2)2 (s) ΔH=-134kJ/mol 2 55 CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O = 2 MPa
【解析】Ⅰ.(1)已知:①2NH3(g)+CO2(g)═H2NCOONH4(s)△H=-272kJmol-1;②H2NCOONH4(s)═CO(NH2)2(s)+H2O(g)△H=+138kJmol-1;根据盖斯定律,①+②可得:2NH3(g)+CO2(g)H2O(g)+CO(NH2)2 (s)△H=-134kJ/mol,故答案为:2NH3(g)+CO2(g)H2O(g)+CO(NH2)2 (s)△H=-134kJ/mol;
(2)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二步反应,从曲线斜率不难看出第2步反应速率慢,所以合成尿素总反应的快慢由第2步反应决定,根据图可知,尿素在55分钟时,物质的量不再变化,即反应达到平衡,所以总反应进行到55min时到达平衡,故答案为:2;55;
(3)电解尿素[CO(NH2)2]的碱性溶液制纯净氢气的过程中同时产生氮气,电解时,阳极上发生氧化反应得到氧化产物,即为氮气,电极反应式为CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O,故答案为:CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O;
Ⅱ.①A、B两点的温度相同,平衡常数K只与温度有关,故浓度平衡常数关系:Kc(A)=Kc(B);故答案为:=;
②1molNO2和足量C发生该反应,设反应二氧化氮x,列三段式:
2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
n始: 1 0 0
n转: x 0.5x x
n平: 1-x 0.5x x
从图知C点时NO2和CO2的物质的量浓度,则1-x=x,解得x=0.5,则平衡时总的物质的量为1.25mol,C点时该反应的压强平衡常数Kp(C)=  =2MPa;故答案为:2MPa。
=2MPa;故答案为:2MPa。

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案