ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΡΩ«ΑΙΛ“ΒΚœ≥…Α±ΒΡ‘≠άμ «ΘΚN2Θ®gΘ©+3H2Θ®gΘ©2NH3Θ®gΘ©ΓςH=©¹93.0kJ/molΘΜ
ΝμΨί±®ΒάΘ§“ΜΕ®ΧθΦΰœ¬ΘΚ2N2Θ®gΘ©+6H2OΘ®lΘ©4NH3Θ®gΘ©+3O2Θ®gΘ©ΓςH=+1530.0kJ/molΘ°
Θ®1Θ©«βΤχΒΡ»Φ…’»»ΓςH=kJ/molΘ°
Θ®2Θ©‘ΎΚψΈ¬Κψ―ΙΉΑ÷Ο÷–Ϋχ––ΙΛ“ΒΚœ≥…Α±Ζ¥”ΠΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ « Θ°
A.ΤχΧεΧεΜΐ≤Μ‘Ό±δΜ·Θ§‘ρ“―ΤΫΚβ
B.ΤχΧεΟήΕ»≤Μ‘Ό±δΜ·Θ§…–Έ¥ΤΫΚβ
C.ΤΫΚβΚσΘ§ΆυΉΑ÷Ο÷–Ά®»κ“ΜΕ®ΝΩArΘ§―Ι«Ω≤Μ±δΘ§ΤΫΚβ≤Μ“ΤΕ·
D.ΤΫΚβΚσΘ§―ΙΥθΉΑ÷ΟΘ§…ζ≥…ΗϋΕύNH3
Θ®3Θ©‘ΎΚψΈ¬Κψ»ίΉΑ÷Ο÷–Ϋχ––Κœ≥…Α±Ζ¥”ΠΘ°
ΔΌ±μ ΨN2≈®Ε»±δΜ·ΒΡ«ζœΏ « Θ°
ΔΎ«Α25min ΡΎΘ§”ΟH2≈®Ε»±δΜ·±μ ΨΒΡΜ·―ßΖ¥”ΠΥΌ¬ « Θ°
Δέ‘Ύ25minΡ©Η’ΚΟΤΫΚβΘ§‘ρΤΫΚβ≥Θ ΐK= Θ°
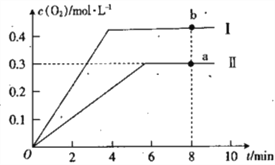
Θ®4Θ©‘ΎΒΎ25min Ρ©Θ§±Θ≥÷ΤδΥϋΧθΦΰ≤Μ±δΘ§…ΐΗΏΈ¬Ε»Θ§‘ΎΒΎ35minΡ©‘Ό¥ΈΤΫΚβΘ°ΤΫΚβ“ΤΕ·Ιΐ≥Χ÷–H2≈®Ε»±δΜ·ΝΥ1.5molL©¹1 Θ§ ‘ΎΆΦ÷–Μ≠≥ωΒΎ25minΓΪ40min NH3≈®Ε»±δΜ·«ζœΏ Θ° 
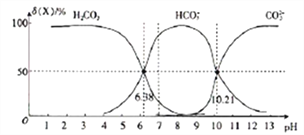
Θ®5Θ©“―÷Σ≥ΘΈ¬œ¬Θ§NH4+ΒΡΥ°Ϋβ≥Θ ΐΈΣ1.0ΓΝ10©¹9 Θ§ ‘ρ0.1mol/L NH4Cl»ή“ΚpH= Θ° Θ®Κω¬‘NH4+Υ°ΫβΕ‘NH4+≈®Ε»ΒΡ”ΑœλΘ©
ΓΨ¥πΑΗΓΩ
Θ®1Θ©©¹286.0
Θ®2Θ©A,D
Θ®3Θ©C,0.12mol/Θ®L?minΘ©,0.15
Θ®4Θ©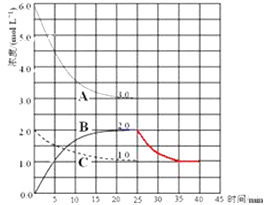
Θ®5Θ©5
ΓΨΫβΈωΓΩΫβΘΚΘ®1Θ©»Φ…’»»ΈΣ1molΈο÷ Άξ»Ϊ»Φ…’ΒΟΒΫΈ»Ε®―θΜ·ΈοΥυ ΆΖ≈ΒΡ»»ΝΩΘ§ΒΎ“ΜΗωΖ¥”ΠΓΝ ![]() ©¹ΒΎΕΰΗωΖ¥”ΠΓΝ
©¹ΒΎΕΰΗωΖ¥”ΠΓΝ ![]() Θ§Φ¥Ω…ΒΟΒΫ«βΤχΒΡ»Φ…’»»ΖΫ≥Χ ΫΘΚH2Θ®gΘ©+
Θ§Φ¥Ω…ΒΟΒΫ«βΤχΒΡ»Φ…’»»ΖΫ≥Χ ΫΘΚH2Θ®gΘ©+ ![]() O2Θ®gΘ©=
O2Θ®gΘ©= ![]() H2OΘ®lΘ©Θ§ΓςH=©¹©¹286.0kJ/molΘ§
H2OΘ®lΘ©Θ§ΓςH=©¹©¹286.0kJ/molΘ§
Υυ“‘¥πΑΗ «ΘΚ©¹286.0ΘΜ
Θ®2Θ©AΘ°Κœ≥…Α±Ζ¥”Π«ΑΚσΤχΧεΧεΜΐ≤ΜΆ§Θ§Β±ΧεΜΐ≤Μ±δ ±Θ§ΒΟΒΫΜ·―ßΤΫΚβΉ¥Χ§Θ§Ι A’ΐ»ΖΘΜ
BΘ° ![]() Θ§ΤχΧε÷ ΝΩ≤Μ±δΘ§”…”ΎΖ¥”Π«ΑΚσΤχΧεΧεΜΐ≤ΜΆ§Θ§Κψ―Ι»ίΤςΤχΧεΧεΜΐΩ…±δΘ§Μ·―ßΤΫΚβ“ΤΕ· ±Θ§ΟήΕ»Υφ÷°±δΜ·Θ§Β±ΟήΕ»≤Μ±δ ±Θ§¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§Θ§Ι B¥μΈσΘΜ
Θ§ΤχΧε÷ ΝΩ≤Μ±δΘ§”…”ΎΖ¥”Π«ΑΚσΤχΧεΧεΜΐ≤ΜΆ§Θ§Κψ―Ι»ίΤςΤχΧεΧεΜΐΩ…±δΘ§Μ·―ßΤΫΚβ“ΤΕ· ±Θ§ΟήΕ»Υφ÷°±δΜ·Θ§Β±ΟήΕ»≤Μ±δ ±Θ§¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§Θ§Ι B¥μΈσΘΜ
CΘ°≥δ»κArΘ§»ίΤς―Ι«Ω≤Μ±δΘ§‘ρΘΚN2ΓΔH2ΓΔΚΆNH3≈®Ε»ΫΒΒΆΘ§Ζ¥”ΠΈο≈®Ε»ΫΒΒΆ¥σΘ§Μ·―ßΤΫΚβœρΡφΖ¥”ΠΖΫœρ“ΤΕ·Θ§Ι C¥μΈσΘΜ
DΘ°ΤΫΚβ ±Θ§―ΙΥθΧεΜΐΘ§―Ι«Ω‘ω¥σΘ§Μ·―ßΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§NH3≈®Ε»‘ω¥σΘ§Ι D’ΐ»ΖΘΜ
Ι ―ΓΘΚADΘΜ
Θ®3Θ©ΔΌΗυΨίΚœ≥…Α±Μ·―ßΖΫ≥Χ Ϋ≈–ΕœΘ§N2ΈΣΖ¥”ΠΈοΘ§«“≈®Ε»±δΜ·±»H2≈®Ε»±δΜ·Ϋœ–ΓΘ§Ω…÷Σ«ζœΏCΈΣN2≈®Ε»ΒΡ±δΜ·«ζœΏΘ§
Υυ“‘¥πΑΗ «ΘΚCΘΜ
ΔΎ«Α25min ΡΎΘ§H2≈®Ε»”…6.0 mol/L±δΈΣ3.0 mol/LΘ§v= ![]() =
= ![]() =0.12 mol/Θ®LminΘ©
=0.12 mol/Θ®LminΘ©
Υυ“‘¥πΑΗ «ΘΚ0.12 mol/Θ®LminΘ©ΘΜ
Δέ25minΡ© ±Θ§N2≈®Ε»ΈΣ1.0mol/LΘ§H2≈®Ε»ΈΣ3.0mol/LΘ§NH3≈®Ε»ΈΣ2.0mol/LΘ§Μ·―ßΤΫΚβ≥Θ ΐΈΣK= ![]() =
= ![]() =0.15Θ§
=0.15Θ§
Υυ“‘¥πΑΗ «ΘΚ0.15ΘΜ
Θ®4Θ©Κœ≥…Α±ΈΣΖ≈»»Ζ¥”ΠΘ§…ΐΗΏΈ¬Ε»Μ·―ßΤΫΚβœρΡφΖ¥”ΠΖΫœρ“ΤΕ·Θ§Φ¥NH3≈®Ε»”…2.0molL©¹1±δΈΣΝΥ1.5molL©¹1Θ§«“Έ¬Ε»Η’…ΐΗΏ ±Θ§≈®Ε»±δΜ·ΫœΩλΘ§
Υυ“‘¥πΑΗ «ΘΚ 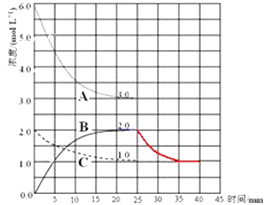 ΘΜ
ΘΜ
Θ®5Θ©Υ°ΫβΖΫ≥Χ ΫΈΣΘΚ ![]() Θ§–¥≥ωΥ°ΫβΤΫΚβ≥Θ ΐ±μ¥ο ΫΈΣΘΚ
Θ§–¥≥ωΥ°ΫβΤΫΚβ≥Θ ΐ±μ¥ο ΫΈΣΘΚ ![]() Θ§«βάκΉ”≈®Ε»”κ“ΜΥ°ΚœΑ±≈®Ε»œύΆ§Θ§Φ¥
Θ§«βάκΉ”≈®Ε»”κ“ΜΥ°ΚœΑ±≈®Ε»œύΆ§Θ§Φ¥ ![]() =1.0ΓΝ10©¹9Θ§[NH4+]=0.1mol/Θ§ΦΤΥψΒΟ[H+]=1.0ΓΝ10©¹5Θ§pH=5Θ§
=1.0ΓΝ10©¹9Θ§[NH4+]=0.1mol/Θ§ΦΤΥψΒΟ[H+]=1.0ΓΝ10©¹5Θ§pH=5Θ§
Υυ“‘¥πΑΗ «ΘΚ5Θ°
ΓΨΩΦΒψΨΪΈωΓΩΙΊ”Ύ±ΨΧβΩΦ≤ιΒΡΜ·―ßΤΫΚβ≥Θ ΐΒΡΚ§“εΚΆΜ·―ßΤΫΚβΉ¥Χ§±Ψ÷ ΦΑΧΊ’ςΘ§–η“ΣΝΥΫβ÷Η‘Ύ“ΜΕ®ΧθΦΰœ¬ΒΡΩ…ΡφΖ¥”ΠάοΘ§’ΐΖ¥”ΠΚΆΡφΖ¥”ΠΒΡΥΌ¬ œύΒ»Θ§Ζ¥”ΠΜλΚœΈο÷–ΗςΉιΖ÷ΒΡ≈®Ε»≤Μ±δΒΡΉ¥Χ§ΘΜΜ·―ßΤΫΚβΉ¥Χ§ΒΡΧΊ’ςΘΚΓΑ»ñ֥ V’ΐ=VΡφ>0ΘΜΓΑΕ·Γ±Φ¥ «Ε·Χ§ΤΫΚβΘ§ΤΫΚβ ±Ζ¥”Π»‘‘ΎΫχ––ΘΜΓΑΕ®Γ±Φ¥Ζ¥”ΠΜλΚœΈο÷–ΗςΉιΖ÷ΑΌΖ÷Κ§ΝΩ≤Μ±δΘΜΓΑ±δΓ±Φ¥ΧθΦΰΗΡ±δΘ§ΤΫΚβ±Μ¥ρΤΤΘ§≤Δ‘Ύ–¬ΒΡΧθΦΰœ¬Ϋ®ΝΔ–¬ΒΡΜ·―ßΤΫΚβΘΜ”κΆΨΨΕΈόΙΊΘ§ΆβΫγΧθΦΰ≤Μ±δΘ§Ω…ΡφΖ¥”ΠΈό¬έ «¥”’ΐΖ¥”ΠΩΣ ΦΘ§ΜΙ «¥”ΡφΖ¥”ΠΩΣ ΦΘ§ΕΦΩ…Ϋ®ΝΔΆ§“ΜΤΫΚβΉ¥Χ§Θ®Β»–ßΘ©≤≈ΡήΒΟ≥ω’ΐ»Ζ¥πΑΗΘ°

 ΩΎΥψ–ΡΥψΥΌΥψ”Π”ΟΧβœΒΝ–¥πΑΗ
ΩΎΥψ–ΡΥψΥΌΥψ”Π”ΟΧβœΒΝ–¥πΑΗ Ά§≤ΫΆΊ’Ι‘ΡΕΝœΒΝ–¥πΑΗ
Ά§≤ΫΆΊ’Ι‘ΡΕΝœΒΝ–¥πΑΗ