��Ŀ����
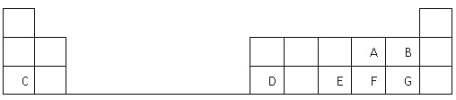
����Ŀ�������ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������
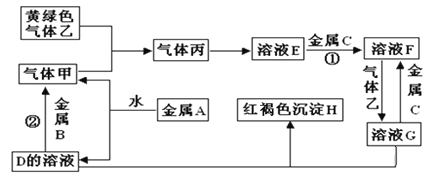
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��H_______________����______________��
��2��д�����з�Ӧ�����ӷ���ʽ
��Ӧ��_________________________________________________________________
��Ӧ��_________________________________________________________________
��3��������ҺG�е������ӣ���ȡ������ҺG���Թ��У��μ�KSCN��Һ��������____________��������ҺG�е������ӣ�����ȡ������ҺG���Թ��У��μ�__________���ѧʽ����Һ�������Dz�����ɫ������
���𰸡� Fe(OH)3 Cl2 Fe+2H+ = Fe2++H2�� 2OH��+2Al+2H2O = 2AlO2��+3H2�� ��Һ��ΪѪ��ɫ AgNO3
������������A��ɫ��ӦΪ��ɫ����AΪ����Na����ˮ��Ӧ����NaOH����������DΪNaOH�������ΪH2���������������B��Ӧ�����������ʽ���BΪAl������ɫ������ΪCl2����������Ӧ���ɱ�ΪHCl��HCl����ˮ������EΪ���ᡣ��������������G��Ӧ���ɺ��ɫ����H��Fe(OH)3��������G�к���Fe3+����ת����ϵHCl��C��Ӧ����F��F��������Ӧ��������G��֪����CΪFe������FΪFeCl2������GΪFeCl3��������ʵ����ʽ����⡣
�������Ϸ�����֪AΪNa��BΪAl��CΪFe��DΪNaOH��E�����ᣬFΪFeCl2��GΪFeCl3��H��Fe(OH)3����ΪH2����ΪCl2����ΪHCl����
��1��ͨ�����Ϸ���֪HΪFe(OH)3����ΪCl2��
��2����Ӧ�����������ᷴӦ�����Ȼ�����������������ʽΪFe+2H+ =Fe2++H2������Ӧ���ǽ�����������������Һ��Ӧ����ƫ�����ƺ�����������ʽΪ2OH��+2Al+2H2O��2AlO2��+3H2����
��3��GΪFeCl3�����е�������Ϊ�����ӣ����������ӳ��õ��Լ���KSCN��Һ����������Һ�Ժ�ɫ���������������ӣ�һ������������Һ���飬�����Dz�����ɫ������

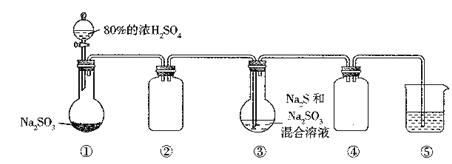
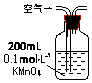
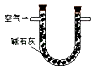
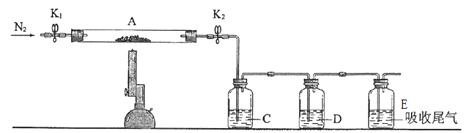
����Ŀ��ij��ȤС������������װ�úͷ����ⶨ������SO2����������Ϊ���еIJ�����
��� | A | B | C |
װ�� |
|
|
|
ԭ�� | ͨ��V���������ⶨ���ɳ��������� | ��KMnO4��Һ�պ���ɫʱ���ⶨͨ����������V | ͨ��V���������ⶨU�����ӵ����� |
����Ŀ���������ı仯�ͷ�Ӧ�Ŀ����ȽǶ��о���ѧ��Ӧ������Ҫ���塣
��1����֪һ�������£���ӦN2+3H2![]() 2NH3Ϊ���ȷ�Ӧ;��
2NH3Ϊ���ȷ�Ӧ;��
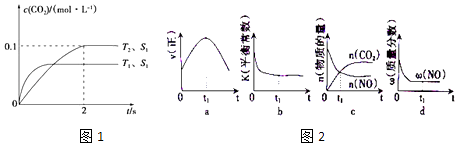
����ͼ����ȷ��ʾ�÷�Ӧ�������仯����________��
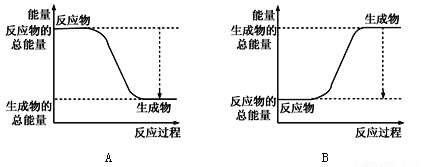
�ڸ����±����ݣ���������1molNH3ʱ�÷�Ӧ�ų�������Ϊ______kJ��
��ѧ�� | H-H | N��N | N-H |
�Ͽ�1mol�������յ����� | 436kJ | 946kJ | 391kJ |
��һ���¶��£���3molH2��1molN2ͨ���ݻ�Ϊ2 L���ܱ������з�����Ӧ����5min�ﵽƽ�⣬���c(NH3)=0.4mol/L����0��5min��N2��ƽ����ѧ��Ӧ����v(N2)=______����Ӧ��ʼ��ƽ��ʱ��������ʵ���֮��Ϊ__________�����ﵽƽ��ʱ���������ڻ��������ѹǿΪp�����������ʼѹǿΪp0 ������p0��p����ʾ�ﵽƽ��ʱH2��ת����Ϊ__________��
�� �ڢ۷�Ӧ�����£��ܹ��жϸ÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬����______________��
A�������ڻ�������ܶȲ���
B����������ѹǿ����
C����λʱ��������n mol N2 ��ͬʱ����2n mol NH3
D�� v (N2)��2v(NH3)
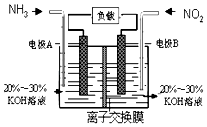
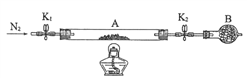
��2��ԭ��ؿɽ���ѧ��ת��Ϊ���ܡ���A��B��C��D���ֽ������±���װ�ý���ʵ�飺

��װ�ü���SO![]() ��________ ���ƶ����A����B������
��________ ���ƶ����A����B������
�����ֽ��������ǿ������˳����_____________��
����װ�ñ��еĵ缫Ϊ������ȵ�������ͭ������ع���һ��ʱ���ȡ��ϴ����������������缫������Ϊ6g��������ͨ�����ӵ����ʵ���Ϊ______mol��