题目内容
【题目】已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-![]() H++B2-,则下列说法中一定正确的是
H++B2-,则下列说法中一定正确的是
A. 在Na2B溶液中一定有:c(OH![]() )=c(H
)=c(H![]() )+c(HB
)+c(HB![]() )+2c(H2B)
)+2c(H2B)
B. NaHB溶液可能存在以下关系:c(Na![]() )>c(HB
)>c(HB![]() )>c(OH
)>c(OH![]() )>c(H
)>c(H![]() )
)
C. NaHB水溶液中一定有:c(Na![]() )+c(H
)+c(H![]() )=c(HB
)=c(HB![]() )+c(OH
)+c(OH![]() )+c(B
)+c(B![]() )
)
D. NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
【答案】D
【解析】酸H2B在水溶液中第一步完全电离,第二步部分电离,所以B2-只能发生一步水解。A.B2-只能发生一步水解,所以溶液中不存在H2B,溶液中存在质子守恒c(OH-)=c(H+)+c(HB-),故A错误;B.HB-在水溶液里只能电离不能水解,导致溶液呈酸性,所以c(OH-)<c(H+),故B错误;C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(HB-) +c(OH-)+2c(B2-),故C错误;D.HB-在水溶液里只能电离不能水解,B2-只能发生一步水解,所以NaHB溶液一定呈酸性,Na2B溶液一定呈碱性,故D正确;故选D。

 应用题作业本系列答案
应用题作业本系列答案【题目】根据题意回答下列问题
(I)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量).
(1)反应的热化学方程式为 .
(2)又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 .
(4)(II)某实验小组测定中和热做了三次实验,所用NaOH溶液的浓度为0.55molL﹣1 , 盐酸的浓度为0.5molL﹣1 , 每次取NaOH溶液和盐酸溶液各50mL,并记录如表原始数据.
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2﹣t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
① | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
② | 25.1 | 25.1 | 25.1 | 28.4 | 3.3 |
③ | 25.1 | 25.1 | 25.1 | 28.5 | 3.4 |
已知盐酸、NaOH溶液密度近似为1.00gcm﹣3 , 中和后混合液的比热容c═4.18×10﹣3 kJg﹣1℃﹣1 , 则该反应的中和热为△H= .
(5)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会(填“偏大”、“偏小”或“不变”),其原因是 .
(6)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热(填“偏大”、“偏小”或“不变”).
【题目】(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
营养成分 | 含量(每100 g) | 营养成分 | 含量(每100 g) |
水分 | 9.9 g | 钙元素 | 23.00 mg |
脂肪 | 0.2 g | 铁元素 | 1.10 mg |
蛋白质 | 4.8 g | 硒元素 | 0.02 mg |
淀粉 | 82.5 g | 花青素 | 0.10 g |
纤维素 | 2.7 g | 其他 | …… |
①以上营养成分中,______是人体中含有的微量元素。
②紫薯粉中的脂肪在人体内会水解成高级脂肪酸和______。
③蛋白质在人体内水解的最终产物是氨基酸,其结构可表示为R—CH(NH2)—X,则“—X”的名称为___。
④在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式______。
(2)合理饮食、正确使用药物对人体健康至关重要。
①“中国居民平衡膳食宝塔”如图所示,位于最上层且每天不超过25g的能量物质是______。
②某品牌饼干的配料标签如图所示,其中苯甲酸钠的作用是______。

③三硅酸镁(Mg2Si3O8·nH2O)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式______。
(3)材料的生产与使用是人类文明和生活进步的一个重要标志。
①我国C919大型客机的机身蒙皮使用的是第三代铝锂合金材料,选用铝锂合金的优点是______(任答一点)。
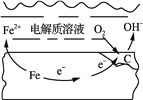
②铁路建设中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一。钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极的电极反应式为______。
③玻璃中加入适量的溴化银(AgBr)和氧化铜的微小晶粒,经过适当的热处理,可以制成变色玻璃,请写出强光照射变色玻璃时发生反应的化学方程式______。