题目内容
碱性锌锰电池的总反应是:Zn + 2MnO2 + 2H2O =" 2MnOOH" + Zn(OH)2,电解质是KOH。下列说法正确的是
| A.MnO2发生了氧化反应 |
| B.MnOOH中Mn元素的化合价为+3 |
| C.反应消耗 0.65gZn,有0.01 mol电子发生转移 |
| D.电池正极的反应为:Zn + 2 OH-–2e-===Zn(OH)2 |
B
根据反应前后的化合价变化可知,二氧化锰中锰的化合价由+4价降低到+3价,所以二氧化锰是氧化剂,发生还原反应,A不正确。锌是还原剂,作负极,发生氧化反应,1mol锌失去2mol电子,C、D不正确。所以答案选B。

练习册系列答案
相关题目
 2 CO32— + 6H2O,则下列说法错误的是
2 CO32— + 6H2O,则下列说法错误的是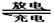 LiFePO4,电解质为导电固体。下列有关LiFePO4电池的说法正确的是
LiFePO4,电解质为导电固体。下列有关LiFePO4电池的说法正确的是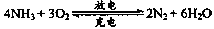

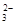 + 12H2O + 14e-;14H2O + 7O2 + 28e-→28OH-,有关推断错误的是( )
+ 12H2O + 14e-;14H2O + 7O2 + 28e-→28OH-,有关推断错误的是( ) ③实验过程中取出盐桥,原电池仍继续工作
③实验过程中取出盐桥,原电池仍继续工作