题目内容
15.实验室可利用乙二醇、铜或铜的化合物制备乙二醛,右图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水,加热装置未画出.试回答:(1)两套装置中的A、B处都需加热,A处用水浴加热,B处用酒精灯加热,A处用水浴加热的主要优点是产生的气流平稳均匀.
(2)若按甲装置进行实验,B管处装铜粉,则通入A管的X是氧气,B中反应的化学方程式为
 .
.(3)若按乙装置进行实验,则B管中应装氧化铜,B中反应的化学方程式为
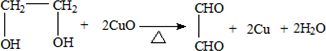 .
.(4)实验结束后,取C试管中的溶液滴入新制备的银氨溶液中并采用水浴加热可观察到有银镜生成,写出该过程的化学方程式
 .
.
分析 (1)醇氧化为醛的条件是铜做催化剂加热;水浴加热优点:受热均匀,可以得到平稳的乙二醇蒸汽;
(2)按甲装置进行实验,B管处装铜粉,则通入A管的X气体为空气或氧气,目的是为了生成氧化铜催化氧化乙二醇生成乙二醛;
(3)按乙装置进行实验无空气或氧气通入,而氧化铜在加热条件下能够氧化乙二醇生成乙二醛;
(4)乙二醛含有醛基,能够被银氨溶液氧化生成单质银、羧酸铵、氨气和水,依据醛基氧化实质写出化学方程式;
解答 解:(1)乙二醇氧化为乙二醛的条件是铜做催化剂加热,可以用酒精灯加热;乙二醇沸点低,加热可以促进乙二醇挥发,用水浴加热,液体受热均匀,产生的乙二醇蒸汽平稳均匀;
故答案为:酒精灯;产生的气流平稳均匀;
(2)按甲装置进行实验,B管处装铜粉,则通入A管的X气体为空气或氧气,目的是为了生成氧化铜催化氧化乙二醇,反应的化学方程式为: ,
,
故答案为:空气或氧气; ;
;
(3)按乙装置进行实验无空气或氧气通入,而氧化铜在加热条件下能够氧化乙二醇生成乙二醛,所以B管中为氧化铜,反应的化学方程式: ,
,
故答案为:氧化铜; ;
;
(4)乙二醛含有醛基,能够被银氨溶液氧化生成单质银、羧酸铵、氨气和水,化学方程式: ,
,
故答案为: .
.
点评 本题通过乙二醛的制备,考查了乙二醇、乙二醛的性质,有机化学方程式的书写,熟悉有机物的结构特点是解题关键,注意醇催化氧化反应的原理,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列各组反应中,最终的溶液中无白色沉淀的是( )
| A. | AlCl3溶液中加入过量氨水 | B. | Al2(SO4)3溶液中加入过量KOH溶液 | ||
| C. | MgCl2溶液中加入过量氨水 | D. | MgSO4溶液中加入过量KOH溶液 |
3.FeSO4•7H2O广泛用于医药和工业领域,实验室制备FeSO4•7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是除去废铁屑表面的油污.
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;
②降低FeSO4在水中的溶解度,减少FeSO4•7H2O的损耗.
(3)FeSO4•7H2O是某些补血剂的主要成分,实验室用KMnO4溶液通过氧化还原滴定测
定某补血剂(1.500g)中铁元素的含量.
①配制100mL 1.200×10 -2mol•L-1的KMnO4溶液时,将溶解后的溶液转移至容 量瓶中的操作方法是用玻璃棒引流,玻璃棒底部要在容量瓶的刻度线以下且玻璃棒不能碰到容量瓶口;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是c.
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在酸式滴定管中.滴定到终点时的现象为滴入最后一滴KMnO4溶液,恰好变为紫红色,且半分钟内不退色.滴定完毕,三次实验记录KMnO4标准溶液的读数如下.
该补血剂中铁元素的质量分数为3.36%.
(4)某实验小组用久置的FeSO4溶液和NaOH溶液制备Fe(OH)2,实验后没有得到预期的白色沉淀,于是采用下列试剂(已煮沸除氧)和装置进行实验:

实验开始打开止水夹C,目的是排除装置中的空气,防止氢氧化亚铁被氧化为氢氧化铁.一段时间后,关闭止水夹C,B中观察到的现象是液面上升出现白色沉淀.B中发生反应的离子方程式是Fe2++2OH-=Fe(OH)2↓.

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是除去废铁屑表面的油污.
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;
②降低FeSO4在水中的溶解度,减少FeSO4•7H2O的损耗.
(3)FeSO4•7H2O是某些补血剂的主要成分,实验室用KMnO4溶液通过氧化还原滴定测
定某补血剂(1.500g)中铁元素的含量.
①配制100mL 1.200×10 -2mol•L-1的KMnO4溶液时,将溶解后的溶液转移至容 量瓶中的操作方法是用玻璃棒引流,玻璃棒底部要在容量瓶的刻度线以下且玻璃棒不能碰到容量瓶口;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是c.
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在酸式滴定管中.滴定到终点时的现象为滴入最后一滴KMnO4溶液,恰好变为紫红色,且半分钟内不退色.滴定完毕,三次实验记录KMnO4标准溶液的读数如下.
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
(4)某实验小组用久置的FeSO4溶液和NaOH溶液制备Fe(OH)2,实验后没有得到预期的白色沉淀,于是采用下列试剂(已煮沸除氧)和装置进行实验:

实验开始打开止水夹C,目的是排除装置中的空气,防止氢氧化亚铁被氧化为氢氧化铁.一段时间后,关闭止水夹C,B中观察到的现象是液面上升出现白色沉淀.B中发生反应的离子方程式是Fe2++2OH-=Fe(OH)2↓.
20.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 用含0.lmolFeCl3的溶液与足量沸水反应制得的Fe(0H)3胶体中胶粒数为0.1NA | |
| B. | 46g N02和N204的混合气体中含原子总数为NA | |
| C. | 标准状况下,5.6L CCl4含有的分子数为0.25NA | |
| D. | 0.25 mol Na2O2中含有的阴离子数为0.5 NA |
7.下列说法错误的是( )
| A. | 乙醇和乙酸都可用于食品调味 | |
| B. | 可以用食醋出去水壶中的水垢(以CaCO3为主) | |
| C. | 乙醇和乙酸都能发生氧化反应 | |
| D. | 酸雨是pH小于7的雨水 |
4.下表为元素周期表的一部分,参照元素①~⑧在表中的位置,用化学用语回答下列问题
(1)④、⑤、⑥的原子半径由大到小的顺序是Na>Al>O.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: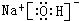 或
或 等.
等.
(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | II A | IIIA | IVA | VA | VIA | VⅡA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
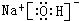 或
或 等.
等.(4)由表中两种元素的原子按1:1组成的常见液态化合物A的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab.a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的上述A溶液,红色很快褪去.褪色原因,甲同学认为A溶液显酸性所致;乙同学认为A溶液强氧化性所致.请你设计一个简单的实验来说明甲对还是乙对.
(简易文字说明)在褪色后的溶液中再逐滴滴入NaOH溶液,若红色不恢复则说明乙对.
5.下列烷烃只有两种同分异构体的是( )
| A. | 丁烷 | B. | 丙烷 | C. | 乙烷 | D. | 戊烷 |
