题目内容
【题目】某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+和Fe3+中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验:

则下列说法正确的是
A. 若含有Fe3+,则一定含有Cl-
B. SO42-、NH4+一定存在,Fe2+和Fe3+可能都存在
C. 该溶液中只存在上述离子中的NO3-、SO42-、NH4+、Fe2+四种离子
D. 气体甲能使湿润的蓝色石蕊试纸变红
【答案】C
【解析】
某溶液X中加入稀硫酸产生气体乙,发生的反应可能是CO32-与H+的反应,也可能是NO3-在H+存在条件下与Fe2+的氧化还原反应;溶液加入过量的氢氧化钠,产生0.02mol气体甲,故溶液中含有NH4+,气体甲是氨气;加入氢氧化钠产生沉淀甲,故溶液中含有Fe2+或Fe3+或两者均有;反应后溶液继续添加氯化钡产生沉淀,故溶液中含有SO42-,沉淀乙为硫酸钡; 根据电荷守恒和题目中要求所含阴离子的物质的量相等,计算具体离子含量,确定NO3-、Cl-存在。
由上述分析可知,产生气体甲0.02mol,则铵根物质的量为0.02mol;产生沉淀乙4.66g,则硫酸根物质的量为0.02mol;沉淀甲为氢氧化铁或氢氧化亚铁或两者均有,经过灼烧后,产物为氧化铁,物质的量为0.01mol,故溶液X中含Fe2+或Fe3+或两者均有,且物质的量一定为0.02mol,由于Fe2+或Fe3+均能与CO32-发生双水解而不能共存,故溶液中无CO32-,则生成气体乙的反应只能是NO3-与Fe2+的氧化还原反应,故溶液中一定含Fe2+和NO3-,而所含阴离子的物质的量相等,即NO3-的物质的量也为0.02mol;
故现在溶液X中已经确定存在的离子是——阴离子:0.02molNO3-,0.02molSO42-,共带0.06mol负电荷;阳离子:0.02molNH4+,0.02molFe2+或Fe2+、Fe3+的混合物,所带的正电荷≥0.06mol,一定不含CO32-。
根据溶液呈电中性可知,当 0.02mol全部是Fe2+时,阳离子所带正电荷为0.06mol,则Cl-不存在;若溶液中含Fe3+,必须存在 Cl-,且物质的量为0.02mol,不符合电中性。
A. 若含有Fe3+,则一定含有Cl-,根据阴离子物质的量相同的条件,氯离子物质的量为0.02mol,无法保持电中性,A错误;
B. SO42-、NH4+ 、Fe2+一定存在,Fe3+一定不存在,B错误;
C. 该溶液中只存在上述离子中的NO3-、SO42-、NH4+、Fe2+四种离子,C正确;
D. 气体甲是氨气,能使湿润的红色石蕊试纸变蓝,D错误;
答案为C。

 每日10分钟口算心算速算天天练系列答案
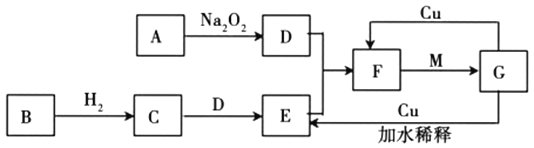
每日10分钟口算心算速算天天练系列答案【题目】某酸性废液含有H+、Fe3+、Ni2+、NO3—、F-和Cr2O72-等。下图是该废液的综合利用工艺流程:(假设: F—与金属离子的络合反应不影响其它反应和计算)
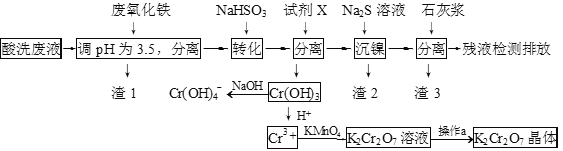
已知:金属离子开始沉淀和沉淀完全时的pH:
Fe3+ | Ni2+ | Cr3+ | |
开始沉淀 | 1.5 | 6.7 | 4.0 |
沉淀完全 | 3.4 | 9.5 | 6.9 |
Ni2+与足量氨水的反应为:Ni2++6NH3 ![]() [Ni(NH3)6]2+([Ni(NH3)6]2+为难电离的络合离子)
[Ni(NH3)6]2+([Ni(NH3)6]2+为难电离的络合离子)
(1)滤渣1的主要成分为:____________。
(2)试剂X可以是足量氨水,还可以是:____________ 。(填序号)
A.Ni(OH)2 B.Cr2O3 C.Fe2O3 D.NaOH
(3)若试剂X是足量氨水,“沉镍”的离子方程式为:____________。
(4)经检测,最后的残液中c(Ca2+)=1.0×10─5 molL-1,则残液中F-浓度____________(填 “符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10-11,国家排放标准要求氟离子浓度小于10 mgL─1]。
(5)镍(Ni)及其化合物广泛应用于生产电池、电镀和催化剂等领域。
①某蓄电池反应为NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2,放电时若外电路中转移0.6mol电子则正极增重____g。
Fe(OH)2+Ni(OH)2,放电时若外电路中转移0.6mol电子则正极增重____g。
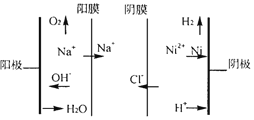
②图为双膜三室电解法处理含镍废水回收金属镍的原理示意图,阳极的电极反应式为____;电解过程中,需要控制溶液pH值为4左右,原因是_______。