题目内容
【题目】电解合成1,2-二氯乙烷的实验装置如图所示。下列说法中不正确的是
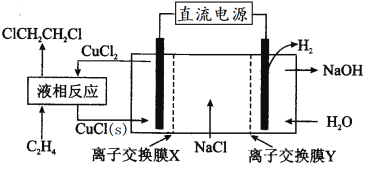
A.该装置工作时,阳极的电极反应是CuCl(s)+Cl--e-=CuCl2
B.液相反应为CH2=CH2+2CuCl2=ClCH2CH2Cl+2CuCl(s)
C.X、Y依次为阳离子交换膜、阴离子交换膜
D.该装置总反应为CH2=CH2+2NaCl+2H2O![]() ClCH2CH2Cl+2NaOH+H2↑
ClCH2CH2Cl+2NaOH+H2↑
【答案】C
【解析】
由图可知,左边电极失电子,铜元素化合价升高,为阳极,发生反应为:CuCl(s)+Cl--e-=CuCl2;
右边电极得电子,氢元素化合价降低,为阴极,发生反应为:2H2O+2e-=H2↑+2OH-。
A.由分析可知,阳极的电极反应是CuCl(s)+Cl--e-=CuCl2,A正确;
B.由图可知,液相反应为CH2=CH2+2CuCl2=ClCH2CH2Cl+2CuCl(s),B正确;
C.Cl-透过X膜在左边电极反应,故X膜为阴离子交换膜,Na+透过Y膜和右边电极附近产生的OH-结合得到NaOH,故Y为阳离子交换膜,C错误;
D.结合装置图可知,该装置总反应为CH2=CH2+2NaCl+2H2O![]() ClCH2CH2Cl+2NaOH+H2↑,D正确。
ClCH2CH2Cl+2NaOH+H2↑,D正确。
答案选C。

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向BaCl2溶液中通入SO2和气体X,出现白色沉淀 | 气体X一定作氧化剂 |
B | NaHCO3溶液与NaAlO2溶液混合,立即产生白色沉淀 | 结合H+的能力:AlO2->CO32- |
C | 向盛有Cu2O的试管中加入足量稀硫酸,溶液变为蓝色,试管底有红色沉淀 | 氧化性:H+>Cu2+ |
D | 向2支盛有2mL0.1mol/LNaOH溶液的试管中分别滴入2滴0.1mol/LAlCl3、MgCl2溶液,振荡,前者无沉淀,后者有白色沉淀 | Ksp[Al(OH)3]>Ksp[Mg(OH)2] |
A.AB.BC.CD.D