题目内容
下列盐既能发生水解反应,蒸干该盐溶液并充分加热后又能得到该盐(加热体系)的是
| A.Na2CO3 | B.AlCl3 | C.NaCl | D.NH4Cl |
A
解析试题分析:A、正确;B、加热时水解产生的HCl挥发,平衡正向移动得到氢氧化铝,错误;C、不水解,错误;D、受热易分解,错误。
考点:考查盐类水解有关问题。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列四种溶液中,室温下由水电离生成的H+浓度之比(①∶②∶③∶④)是( )
①pH=0的盐酸
②0.1 mol·L-1的盐酸
③0.01 mol·L-1的NaOH溶液
④pH=11的NaOH溶液
| A.1∶10∶100∶1 000 | B.0∶1∶12∶11 |
| C.14∶13∶12∶11 | D.14∶13∶2∶3 |
W、X、Y、Z是原子序数依次增大的四种短周期元素,化合物WX能抑制水的电离,离子化合物Y2Z能捉进水的电离。则Y元素是
| A.Li | B.F | C.Na | D.Cl |
用0.10 mol/L 的盐酸滴定0.10 mol/L 的氨水,滴定过程中不可能出现的结果是
A.c(NH4+)>c(Cl ),c(OH ),c(OH )>c(H )>c(H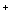 ) ) | B.c(NH4+) = c(Cl ),c(OH ),c(OH ) = c(H ) = c(H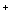 ) ) |
C.c(Cl )>c(NH4+),c(OH )>c(NH4+),c(OH )>c(H )>c(H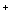 ) ) | D.c(Cl )>c(NH4+),c(H )>c(NH4+),c(H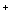 )>c(OH )>c(OH ) ) |
关于强弱电解质的叙述正确的是:( )
| A.强电解质都是离子化合物,弱电解质都是共价化合物 |
| B.强电解质都是可溶性化合物,弱电解质都是难溶性化合物 |
| C.弱电解质的水溶液的导电能力比强电解质溶液弱 |
| D.强电解质的稀溶液中无溶质分子,弱电解质的溶液中存在溶质分子 |
常温下amo1/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判断一定错误的是
| A.c(OH一)>c(H+)时,a=b | B.c(K+)>c(CH3COO—)时,a>b |
| C.c(OH一)=c(H+)时,a>b | D.c(K+)<c(CH3COO—)时,a<b |
等物质的量浓度的下列四种溶液中, 浓度最大的是( )
浓度最大的是( )
| A.NH4Cl | B.NH4HCO3 | C.NH4NO3 | D.NH4HSO4 |
对水的电离平衡一定不产生影响的微粒是
A. | B. | C.1s22s22p6 | D.K+ |
用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中,不会引起实验误差的是
| A.用蒸馏水冼净滴定管后,装入标准盐酸进行滴定 |
| B.用蒸馏水冼净锥形瓶后,再用NaOH液润洗,而后装入一定体积的NaOH溶液 |
| C.用甲基橙做指示剂,当溶液由黄色变成橙色,立刻读数盐酸体积。 |
| D.用碱式滴定管取10.00 mLNaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量蒸馏水进行滴定 |