题目内容
【题目】天然气是重要的化石能源,其综合利用的研究意义重大。
已知;i.CH4(g)十H2O(g)![]() CO(g)+3H2(g) H=+206kJmol-1;
CO(g)+3H2(g) H=+206kJmol-1;
ii.CH4(g)+2H2O(g)![]() CO2(g)+4H2(g) H=+165kJmol-1;
CO2(g)+4H2(g) H=+165kJmol-1;
iii.C(s)十H2O(g)![]() CO(g)十H2(g) H=+131.4kJmol-1。
CO(g)十H2(g) H=+131.4kJmol-1。
请回答下列问题:
(1)若将物质的量之比为1:1的CH4(g)和H2O(g)充入密闭容器中发生反应i。CH4(g)和CO(g)的平衡体积分数(φ)与温度(T)的关系如图所示:
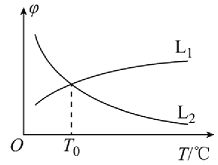
图中表示CH4(g)的平衡体积分数与温度关系的曲线为___(填“L1”或“L2”),原因为__。
(2)合成气的主要组分为CO和H2;以天然气为原料生产的合成气有多种方法,其中Sparg工艺的原理为CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
2CO(g)+2H2(g) H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
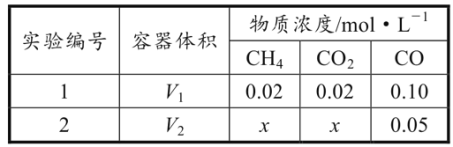
①H1=__。
②T℃下,该反应的平衡常数K=__。
③实验1中,CO的平衡体积分数为__%(保留三位有效数字)。
④V1:V2=_。
(3)甲烷在高温下分解生成的炭黑,是生成橡胶的重要原料,其分解原理为CH4(g)![]() C(s)+2H2(g)。
C(s)+2H2(g)。
①一定温度下,将n1molCH4充入1L恒容密闭容器中发生上述反应,tmin末容器内压强变为原来的1.6倍。tmin内该反应的平均反应速率v(H2)=__(用含n1和t的代数式表示)。
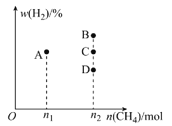
②若控制温度和压强不变,充入CH4的物质的量与平衡时H2的体积分数的关系如图所示。充入n1molCH4时,平衡点位于A点,则充入n2molCH4时,平衡点位于__(填“B”“C”或“D”)点。
【答案】L2 反应i为吸热反应,温度升高平衡正向进行甲烷体积分数降低; +247kJ/mol 0.25 41.7 3:7 ![]() mol/(Lmin) C
mol/(Lmin) C
【解析】
(1)反应i为吸热反应,图1中表示甲烷的平衡体积分数与温度关系的曲线为L2;
(2)①由盖斯定律计算H1
②T℃下,该反应的平衡常数K=![]() ,由图表数据计算得到;
,由图表数据计算得到;
③实验1中生成CO物质的量浓度=0.10mol/L,平衡状态下气体总浓度=0.02mol/L+0.02mol/L+0.1mol/L+0.1mol/L=0.24mol/L,据此计算CO的平衡体积分数;
④平衡常数随温度变化,利用平衡常数列式计算,![]() =0.25,x=0.005,假设平衡时的体积不变,将实验1和实验2中的平衡状态利用极值可以得到,当c(CO)=0mol/L时,实验1中c(CH4)=0.07mol/L,实验2中c(CH4)=0.03mol/L,而此时两个虚拟容器中甲烷的物质的量相同,物质的量浓度之比等于体积的反比;
=0.25,x=0.005,假设平衡时的体积不变,将实验1和实验2中的平衡状态利用极值可以得到,当c(CO)=0mol/L时,实验1中c(CH4)=0.07mol/L,实验2中c(CH4)=0.03mol/L,而此时两个虚拟容器中甲烷的物质的量相同,物质的量浓度之比等于体积的反比;
(3)①tmin②末容器内压强变为原来的1.6倍,气体物质的量变为原来的1.6倍为1.6n1mol,其中n(H2)=1.2n1mol,tmin内该反应的平均反应速率v(H2)=![]() ;
;
②若控制温度和压强不变,只改变甲烷的物质的量,平衡时氢气的体积分数不变。
(1)图1中表示甲烷的平衡体积分数与温度关系的曲线为L2,原因是反应i为吸热反应,温度升高平衡正向进行甲烷体积分数降低,故答案为:L2;反应i为吸热反应,温度升高平衡正向进行甲烷体积分数降低;
(2)①已知:i.CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206kJmol-1;
ii.CH4(g)+2H2O(g)CO2(g)+4H2(g)△H=+165kJmol-1;
盖斯定律计算i×2-ii得到:CH4(g)+CO2(g)2CO(g)+2H2(g)△H1=+247kJ/mol,故答案:+247kJ/mol;
②T℃下,该反应的平衡常数K=![]() =
=![]() =0.25,故答案为:0.25;
=0.25,故答案为:0.25;
③实验1中生成CO物质的量浓度=0.10mol/L,平衡状态下气体总浓度=0.02mol/L+0.02mol/L+0.1mol/L+0.1mol/L=0.24mol/L,CO的平衡体积分数=![]() ×100%=41.7%,故答案为:41.7;
×100%=41.7%,故答案为:41.7;
④利用平衡常数列式计算,![]() =0.25,x=0.005,假设平衡时的体积不变,将实验1和实验2中的平衡状态利用极值可以得到,当c(CO)=0mol/L时,实验1中c(CH4)=0.07mol/L,实验2中c(CH4)=0.03mol/L,而此时两个虚拟容器中甲烷的物质的量相同,则物质的量浓度之比等于体积反比,V1:V2=3:7,故答案为:3:7;
=0.25,x=0.005,假设平衡时的体积不变,将实验1和实验2中的平衡状态利用极值可以得到,当c(CO)=0mol/L时,实验1中c(CH4)=0.07mol/L,实验2中c(CH4)=0.03mol/L,而此时两个虚拟容器中甲烷的物质的量相同,则物质的量浓度之比等于体积反比,V1:V2=3:7,故答案为:3:7;
(3)①tmin②末容器内压强变为原来的1.6倍,气体物质的量变为原来的1.6倍为1.6n1mol,其中n(H2)=1.2n1mol,tmin内该反应的平均反应速率v(H2)=![]() mol/(Lmin),故答案为:
mol/(Lmin),故答案为:![]() mol/(Lmin);
mol/(Lmin);
②若控制温度和压强不变,只改变甲烷的物质的量,平衡时氢气的体积分数不变,平衡点在C点,故答案为:C。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案