题目内容
(12分)
某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由 。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4/3% H2O2、6 mol·L-1HNO3/0.01 mol·L-1KmnO4、NaOH稀溶液、0.1 mol·L-1Kl、20% KSCN、蒸馏水。
①提出合理假设:
假设1: ;
假设2: ;
假设3: 。
②设计实验方案证明你的假设(不要在答题卡上作答)。
③实验过程:
根据②的实验方案,进行实验。请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由 。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4/3% H2O2、6 mol·L-1HNO3/0.01 mol·L-1KmnO4、NaOH稀溶液、0.1 mol·L-1Kl、20% KSCN、蒸馏水。
①提出合理假设:
假设1: ;
假设2: ;
假设3: 。
②设计实验方案证明你的假设(不要在答题卡上作答)。
③实验过程:
根据②的实验方案,进行实验。请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 | 预期现象与结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: | |
| … | |
(1)该结论不正确。稀HNO3有强氧化性,若该铁的价态为+2价,则被氧化为+3价同样可使KSCN溶液变血红色。
(2)①提出合理假设
假设1:催化剂中铁元素的价态为+3价。
假设2:催化剂中铁元素的价态为+2价。
假设3:催化剂中铁元素的价态既有+3价也有+2价。
②设计实验方法证明你的假设
③实验过程:
(2)①提出合理假设
假设1:催化剂中铁元素的价态为+3价。
假设2:催化剂中铁元素的价态为+2价。
假设3:催化剂中铁元素的价态既有+3价也有+2价。
②设计实验方法证明你的假设
③实验过程:
| 实验操作 | 预期现象与结论 |
| 步骤1:将适量稀H2SO4加入少许样品于试管中,加热溶解; | 溶液呈黄绿色,说明溶液中含Fe2+或Fe3+。 |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液。 | 若KMnO4溶液的紫红色褪去为无色溶液,则说明催化剂中铁元素的价态含+2价;若不褪色,则说明催化剂中铁元素的价态不含+2价。 |
| 步骤3:另取少量溶液,滴加KSCN溶液。 | 若溶液变为血红色,则说明催化剂中铁元素的价态含+3价;若溶液无明显变化,则说明催化剂中铁元素的价态不含+3价。 |
略

练习册系列答案
相关题目


 。
。 的NaOH溶液刚好使溶液中Cu2+全部沉淀。据此,他能求出余酸的物质的量浓度吗?若能,请写出余酸物质的量浓度的表达式: mol/L(
的NaOH溶液刚好使溶液中Cu2+全部沉淀。据此,他能求出余酸的物质的量浓度吗?若能,请写出余酸物质的量浓度的表达式: mol/L( 用含a的代数式表达,若不能,该空不填)。
用含a的代数式表达,若不能,该空不填)。
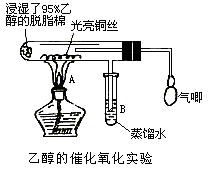 (1)甲同学其实验操作为:预先使棉花团浸透乙醇,并按下图搭好实验装置;在铜丝的中间部分加热,片刻后开始有节奏(间歇性)地鼓入空气,即可观察到明显的实验现象。
(1)甲同学其实验操作为:预先使棉花团浸透乙醇,并按下图搭好实验装置;在铜丝的中间部分加热,片刻后开始有节奏(间歇性)地鼓入空气,即可观察到明显的实验现象。