题目内容
下列事实,不能用勒夏特列原理解释的是( )
A.对2HI(g) H2(g)+I2(g),平衡体系增大压强可使颜色变深 H2(g)+I2(g),平衡体系增大压强可使颜色变深 |
B.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 |
C.CO+NO2 CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 |
| D.往H2S水溶液中加碱有利于S2-的增加 |
A
试题分析:A项:2HI(g)
 H2(g)+I2(g)反应前后总的体积不变,压强对化学平衡没有影响,故选A。
H2(g)+I2(g)反应前后总的体积不变,压强对化学平衡没有影响,故选A。点评:本题考查的是勒夏特列原理的应用,学生需要值得注意的是只有化学平衡移动,才能用勒夏特列原理来解释。

练习册系列答案
相关题目
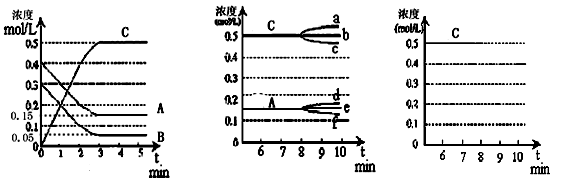
 ,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=
,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=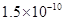
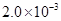 mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:

 mol·L-1HF溶液与
mol·L-1HF溶液与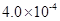 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。
mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。 b B(g)+c C(g),达平衡后,保持温度不变,将容器体积扩大为原来的一倍,当达到新的平衡时,c(A)变为原平衡的40%,下列说法正确的是
b B(g)+c C(g),达平衡后,保持温度不变,将容器体积扩大为原来的一倍,当达到新的平衡时,c(A)变为原平衡的40%,下列说法正确的是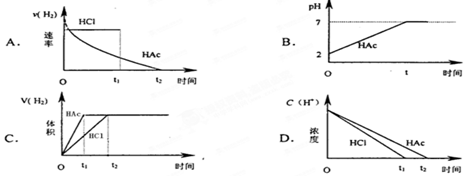
 H2O(g) + CO(g),反应所处的温度相同,但起始浓度不同,其中 甲:n(CO2)=n(H2)=1 mol;乙:n(CO2)=1 mol, n(H2)=2mol;丙:n(CO2)=n(H2)=1mol n[H2O(g)]=1 mol.达到平衡时CO的物质的量由大到小的顺序是( )
H2O(g) + CO(g),反应所处的温度相同,但起始浓度不同,其中 甲:n(CO2)=n(H2)=1 mol;乙:n(CO2)=1 mol, n(H2)=2mol;丙:n(CO2)=n(H2)=1mol n[H2O(g)]=1 mol.达到平衡时CO的物质的量由大到小的顺序是( )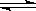 Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26
Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26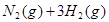
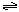
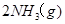
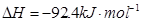 。现
。现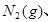 3mol
3mol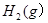 充入一容积为2L的密闭容器中,在500℃下进行反应,10min
充入一容积为2L的密闭容器中,在500℃下进行反应,10min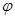 ,下列说法中正确的是( )
,下列说法中正确的是( )