题目内容
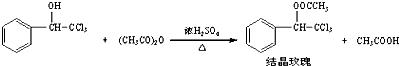
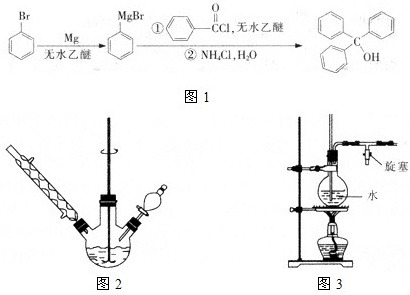
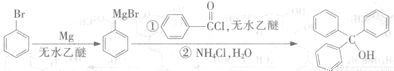
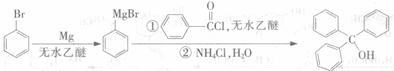
三苯甲醇(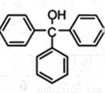 )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示。
已知:i)格氏试剂容易水解,

ii)相关物质的物理性质如下:
|
物质 |
熔点(℃) |
沸点(℃) |
溶解性 |
|
三苯甲醇 |
164.2 |
380 |
不溶于水,溶于乙醇、乙醚等有机溶剂 |
|
乙醚 |
—116.3 |
34.6 |
微溶于水,溶于乙醇、苯等有机溶剂 |
|
溴苯 |
—30.7 |
156.2 |
不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
|
苯甲酸乙酯 |
—34.6 |
212.6 |
不溶于水 |
|
Mg(OH)Br |
常温下为固体 |
能溶于水,不溶于醇、醚等有机溶剂 |
iii)三苯甲醇的相对分子质量是260,纯净固体有机物一般都有固定熔点。
请回答以下问题:
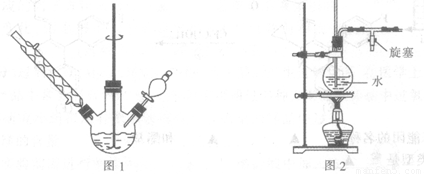
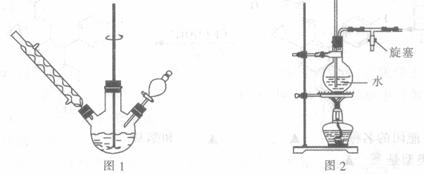
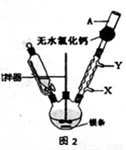
(1)实验室合成三苯甲醇的装置图2,写出玻璃仪器A的名称: ,装有无水CaCl2的仪器A的作用是: ;
(2)制取格氏试剂时要保持微沸,可以采用水浴加热,优点是 ,微沸回流时冷凝管中水流的方向是: (填“X→Y”或“Y→X”);
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等 杂质,可以设计如下提纯方案,请填写空白:
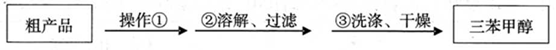
其中,操作①为: ;洗涤液最好选用: ;
A.水 B.乙醚 C.乙醇 D.苯
检验产品已经洗涤干净的操作为: ;
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80m L(标准状况)。产品中三苯甲醇质量分数为 (保留两位有效数字,已知三苯甲醇的分子式为C19H16O,相对分子质量为260)。
(18分)(1)干燥管(2分) 防止空气中水蒸气进入装置(2分)
(2)受热均匀,温度易于控制(2分) X→Y(2分)
(3)蒸馏(或分馏,2分) A(2分) 取最后一次洗出液于试管中,滴加AgNO3溶液,若无白色沉淀生成,则已经洗涤干净(3分)
(4)90%(3分)
【解析】
试题分析:(1)读图2可得,A是干燥管;因为格林试剂容易水解,无水氯化钙是中性干燥剂,主要是防止空气中水蒸气进入装置, 防止格林试剂水解,导致三本甲醇的产量降低;(2)由于水的沸点为100℃,水浴可以控制加热的温度不超过100℃,且可以使反应均匀受热;冷凝管中冷却水采取逆流原理,水流方向是低进高出,即沿X→Y的方向流动;(3)读已知信息ii)中有关物质的物理性质,三苯甲醇、乙醚、溴苯、苯甲酸乙酯是互溶液体混合物,但各组成成分的沸点相差较大,因此粗产品分离的方法是蒸馏或分馏,则操作①是蒸馏或分馏,目的是除去乙醚、溴苯、苯甲酸乙酯等杂质;由于碱式溴化镁能溶于水,不溶于醇、醚等有机溶剂,则操作②的目的是除去碱式溴化镁;由于三苯甲醇不溶于水,溶于乙醇、乙醚等有机溶剂,因此洗涤液最好选择水,不能选择乙醚、乙醇、苯等有机溶液,防止又引入乙醚、乙醇、苯等新的杂质;多余的水可以用无水氯化钙等干燥剂除去,再次蒸馏即可得到纯净的三本甲醇;由于合成流程图中加入氯化铵饱和溶液,沉淀的主要成分是碱式溴化镁, 沉淀具有吸附可溶性离子的性质,则沉淀表面可能吸附着氯离子或铵根离子,根据氯离子的性质可以设计实验方案检验沉淀是否洗涤干净,即取最后一次洗出液于试管中,滴加AgNO3溶液,若无白色沉淀生成,则已经洗涤干净;(4)由于氢气的体积=100.80mL=0.1008L,标准状况下气体摩尔体积为22.4L/mol,n=V/Vm,则氢气的物质的量=0.1008L÷22.4L/mol;由于三苯甲醇只含有1个羟基,由于2mol羟基与2molNa发生置换反应,生成1molH2,则1mol三苯甲醇与足量Na反应最多放出0.5mol H2,即三苯甲醇的物质的量是氢气的2倍,则三苯甲醇的物质的量为0.1008L÷22.4L/mol×2;由于三苯甲醇的分子式为C19H16O,相对分子质量为260,m=n•M,则产品中三苯甲醇的质量为0.1008L÷22.4L/mol×2×260g/mol=2.34g,由于产品的质量为2.60g,则产品中三苯甲醇的质量分数为2.34g÷2.60g×100%=90%。
考点:考查综合实验及化学计算,涉及常用仪器的名称、干燥剂的作用、水浴加热的优点、冷凝管中冷却水的流向、混合物分离提纯的方法、洗涤液的选择、沉淀洗涤干净的方法、物质的量在化学方程式中的应用、气体体积、气体摩尔体积、物质的量、摩尔质量、三苯甲醇的质量和纯度计算、有效数字的处理等。

 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案