题目内容
氢化钠(NaH)是一种白色离子晶体,其中钠是+1价,NaH与水反应放出H2,下列叙述中正确的是
| A.NaH在水中显酸性 |
| B.NaH中氢离子的电子层排布与氦原子相同 |
| C.NaH中氢离子半径比锂离子半径小 |
| D.NaH中氢离子可被还原成H2 |
B
题目中给出的新信息有:①氢化钠的化学式NaH;②NaH是离子晶体;③NaH晶体是白色的;④NaH中Na是+1价;⑤NaH与水反应放出H2。其中③是与解答本题无关的信息,④中强调Na是+1价,其隐蔽潜在的信息是说NaH中H为-1价,NaH是由Na+和H-构成的离子化合物。这个潜在信息是解答本题的关键,把它与学过的离子结构、半径比较、氧化-还原反应等知识联系起来,问题就迎刃而解了。NaH和H2O反应放出H2,是NaH中-1价的H与H2O中+1价的 H发生氧化-还原反应,H-被氧化;NaH+H2O==NaOH+H2↑,水溶液呈碱性。H-的核外电子排布与He、Li+等相同,随着核电荷的递增,半径逐渐变小,VH->VLi+。所以B是答案。

练习册系列答案
相关题目
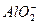 +2H2O
+2H2O