题目内容
【题目】关于下图所示转化关系(X代表卤素),说法不正确的是
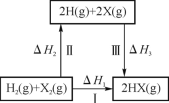
A.2H(g) +2X(g) == 2HX(g) ΔH3<0
B.途径Ⅰ生成HX的反应热与途径无关,所以ΔH1 = ΔH2 + ΔH3
C.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多
D.途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定
【答案】C
【解析】
试题分析:A、卤素和氢气化合是放热反应,所以正确,不选A;B、遵循盖斯定律,反应热与途径无关,所以正确,不选B;C、Cl、Br、I的非金属性依次减弱,单质的稳定性逐渐减弱,所以途径Ⅱ吸收的热量依次减小,错误,选C;D、途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl的能量低,、比HBr稳定,正确,不选D。

【题目】下列实验操作规范并能达到实验目的的是
实验操作 | 实验目的 | |
A | 在一定条件下,向混有少量乙烯的乙烷中通入氢气 | 除去乙烷中的乙烯 |
B | 用玻璃管蘸取待测液,点在干燥的pH试纸中部,片刻后与标准比色卡比较读数 | 粗略测定NaClO溶液pH |
C | 用0.1 mol/LMgSO4溶液滴入到2mlNaOH溶液中至不再有沉淀生成再滴入0.1 mol/LCuSO4溶液 | 比较Mg(OH)2和Cu(OH)2的Ksp大小 |
D | 向亚硫酸钠溶液中滴加硝酸钡和硝酸 | 检验亚硫酸钠溶液是否变质 |
A.AB.BC.CD.D
【题目】碳及其化合物有许多用途。回答下列问题:
⑴碳元素有12C、13C和14C等核素。下列对12C基态原子结构的表示方法中,对电子运动状态描述最详尽的是_______(填标号)。
A. B.
B.![]()
C.1s22s22p2 D.
基态13C原子核外有________种不同空间运动状态的电子。
⑵K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键的类型为________,该化学键能够形成的原因是________。
⑶有机物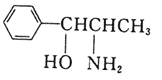 是________(填“极性”或“非极性”)分子;该有机物中存在sp3杂化的原子,其对应元素的第一电离能由大到小的顺序为________。
是________(填“极性”或“非极性”)分子;该有机物中存在sp3杂化的原子,其对应元素的第一电离能由大到小的顺序为________。
⑷乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)3]均属于胺,两者相对分子质量接近,但乙二胺比三甲胺的沸点高得多,原因是________。
⑸碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径:
碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
金属阳离子半径/pm | 66 | 99 | 112 | 135 |
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是________。
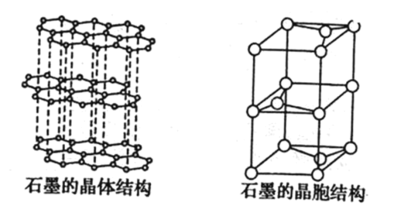
⑹石墨的晶体结构和晶胞结构如图所示。已知石墨的密度为ρgcm-3,C—C键长为γ cm,阿伏加德罗常数的值为NA,则石墨晶体的层间距为________cm。