题目内容
化学中常借助曲线图来表示某种变化过程,有人分别画出了下列的四个曲线图:
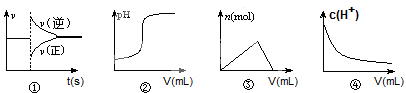
有关上述曲线图的说法正确的是:

有关上述曲线图的说法正确的是:
| A.曲线图①可以表示恒压容器中某化学平衡体系充入气体生成物后反应速率随时间的变化 |
| B.曲线图②可以表示向一定量的氢氧化钠溶液中滴加一定浓度的盐酸时的pH的变化 |
| C.曲线图③可以表示向一定量的明矾溶液中滴加一定浓度的氢氧化钡溶液时的产生沉淀的物质的量变化 |
| D.曲线图④可以表示冰醋酸加水稀释过程中溶液中c(H+)的变化 |
A
试题分析:A、恒压条件下,充入气体生成物,生成物浓度增大,反应物浓度减小,平衡左移,故A正确;B、向一定量的氢氧化钠溶液中滴加一定浓度的盐酸时pH应该减小,错误;C、向一定量的明矾溶液中滴加一定浓度的氢氧化钡溶液时,先产生沉淀,后沉淀会溶解一部分,但不会完全消失,错误;D、冰醋酸加水稀释过程中溶液中c(H+)先增大后减小,错误。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
 2I-+SO42—+4H+
2I-+SO42—+4H+ +2H2O
+2H2O 4OH-+O2↑
4OH-+O2↑ +4H+
+4H+
 Ca2+ + 2OH-
Ca2+ + 2OH- Fe (OH)3(胶体)+3HCl
Fe (OH)3(胶体)+3HCl +2H+ =CO2↑+H2O
+2H+ =CO2↑+H2O =" " BaSO4↓
=" " BaSO4↓ 可用铝粉除去。已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3·H2O、H2O六种物质。
可用铝粉除去。已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3·H2O、H2O六种物质。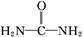 )与N
)与N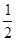 H2SO4(l)+ KOH(l) =
H2SO4(l)+ KOH(l) =  SO2↑+Cu2+ +SO42-+2 H2O
SO2↑+Cu2+ +SO42-+2 H2O