题目内容
黄铜矿(CuFeS2)常用于提炼金属铜。黄铜矿焙烧过程中所发生的反应比较复杂,其中主要反应之一的化学方程式为2CuFeS2+O2=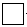 +2FeS+SO2(已配平),则下列关于该反应的说法错误的是
+2FeS+SO2(已配平),则下列关于该反应的说法错误的是
| A.方框中的物质应为Cu2S |
| B.该反应的部分产物可用于硫酸工业 |
| C.反应中SO2既是氧化产物又是还原产物 |
| D.反应中若有1molSO2生成,则一定有4mol电子发生转移 |
D
解析试题分析:A根据质量守恒定律可知方框中的物质为硫化亚铜,正确。B因为产生了二氧化硫,所以可用于工业制取硫酸,正确。C硫化合价从CuFeS2-2→SO2的+4,化合价升高,失去电子,作还原剂,SO2是氧化产物;氧元素的化合价从O2的0,→SO2的-2,化合价降低,得到电子,作氧化剂,SO2是还原产物。正确。D在该反应中,若有1molSO2生成,则有6mol电子发生转移.错误。
考点:考查黄铜矿的应用及涉及的氧化还原反应的等相关知识。

 中考解读考点精练系列答案
中考解读考点精练系列答案根据下列各反应,判断有关物质还原性由强到弱的顺序是( )
① H2SO3+I2+H2O = 2HI + H2SO4
② 2FeCl3+2HI=2FeCl2 + 2HCl + I2
③ 3FeCl2 + 4HNO3=2FeCl3 + NO↑ + 2H2O +Fe(NO3)3
| A.FeCl2>HI>H2SO3>NO | B.H2SO3>HI>FeCl2>NO |
| C.I2>FeCl2>H2SO3>NO | D.NO>FeCl2>H2SO3>HI |
工业制ClO2的化学反应:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4,下列说法正确的是
| A.NaClO3在反应中化合价降低,失去电子 |
| B.SO2在反应中发生氧化反应 |
| C.1mol氧化剂在反应中得到2mol电子 |
| D.H2SO4 在反应中作氧化剂 |
下列过程中涉及化学变化,且属于氧化还原反应的是
| A.家庭中经常用食醋浸泡有水垢的水壶 |
| B.甘油加水作护肤剂 |
| C.烹鱼时,加入少量的酒和食醋可减少腥味,增加香味 |
| D.交通警察用酸性重铬酸钾检查司机是否酒后驾车 |
下列粒子不具有氧化性的是
| A.Cl2 | B.H+ | C.Mg | D.CO2 |
根据下列化学方程式,判断有关物质的还原性强弱顺序正确的是
①I2+SO2+2H2O=H2SO4+2HI;②2FeCl2+Cl2=2FeCl3;③2FeCl3+2HI=2FeCl2+2HCl+I2
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |
苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。若榨汁时加入维生素C,可以有效防止这种现象发生。这说明维生素C具有( )。
| A.氧化性 | B.还原性 | C.碱性 | D.酸性 |
在下列物质间的反应中,酸既表现出氧化性又表现出酸性的是
| A.浓盐酸和高锰酸钾 | B.浓硝酸和铜屑 | C.稀硝酸和SO2 | D.浓硫酸和碳 |
Cu2O呈红色,在酸性条件下会发生自身氧化还原反应。用H2还原CuO所得产物呈红色,若要检验其中是否含有Cu2O,以下试剂选择和判断方法均正确的是:
| 选项 | 试剂 | 判断方法 |
| A | 稀硝酸 | 是否生成蓝色溶液 |
| B | 稀硫酸 | 固体物质是否完全溶解 |
| C | 浓硫酸 | 是否有无色气体生成 |
| D | 稀盐酸 | 是否生成蓝色溶液 |