题目内容
取体积相同的两份0.1mol·L-1的NaOH溶液把其中的一份敞口放在空气中一段时间后,溶液的pH将______(填增大、减小或不变)。用已知浓度的H2SO4溶液去中和两份NaOH溶液时,若中和在空气中放置的溶液所消耗H2SO4溶液体积为V1,另一份消耗H2SO4溶液体积为V2。
(1)以甲基橙为指示剂时,V1和V2的关系是______。
(2)以酚酞作为指示剂时,V1和V2的关系是______。
(1)以甲基橙为指示剂时,V1和V2的关系是______。
(2)以酚酞作为指示剂时,V1和V2的关系是______。
变小 ①V1=V2 ②V1<V2
一份NaOH溶液暴露在空气中,会吸收空气中的CO2气体而转化为Na2CO3,方程式为2NaOH+CO2====Na2CO3+H2O。由于消耗了NaOH,则溶液的pH会减小,该溶液中的溶质为NaOH和Na2CO3,另一份溶液的溶质仍为NaOH。
(1)若以甲基橙为指示剂,变色时溶液呈酸性,则Na2CO3与H2SO4反应转变为CO2溶解在H2O中生成H2CO3而使溶液呈酸性。由于1mol NaCO3由2mol NaOH转变而来,而此时1mol Na2CO3消耗的H2SO4与2mol NaOH消耗的H2SO4相等,所以,V1=V2。
(2)若以酚酞为指示剂,变色时溶液呈弱碱性,Na2CO3与H2SO4反应后应生成NaHCO3,由于NaHCO3溶液中HCO3-水解生成OH-的能力大于HCO3-电离生成H+的能力,从而使溶液呈弱碱性。由于1mol Na2CO3转变为NaHCO3消耗的H2SO4少于2mol NaOH转变为Na2SO4消耗的H2SO4少,所以V1<V2。
(1)若以甲基橙为指示剂,变色时溶液呈酸性,则Na2CO3与H2SO4反应转变为CO2溶解在H2O中生成H2CO3而使溶液呈酸性。由于1mol NaCO3由2mol NaOH转变而来,而此时1mol Na2CO3消耗的H2SO4与2mol NaOH消耗的H2SO4相等,所以,V1=V2。
(2)若以酚酞为指示剂,变色时溶液呈弱碱性,Na2CO3与H2SO4反应后应生成NaHCO3,由于NaHCO3溶液中HCO3-水解生成OH-的能力大于HCO3-电离生成H+的能力,从而使溶液呈弱碱性。由于1mol Na2CO3转变为NaHCO3消耗的H2SO4少于2mol NaOH转变为Na2SO4消耗的H2SO4少,所以V1<V2。

练习册系列答案
相关题目
 、
、 、
、 、
、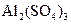 、
、 五种物质中:
五种物质中:
 O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1
O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1 O2(g)===4CO(g)+5H2O(l) ΔH=-1 746 kJ·mol-1
O2(g)===4CO(g)+5H2O(l) ΔH=-1 746 kJ·mol-1