题目内容
12.下列实验操作或对实验事实的描述中,正确的是①③(填序号).①用量筒量取稀硫酸溶液8.0mL;
②Fe(OH)3胶体与FeCl3溶液的混合物可用过滤的方法分离;
③用湿润的pH试纸测量某溶液pH时,测量值可能比真实值小;
④用碱式滴定管量取KMnO4溶液20.50mL;
⑤在实验室中用锌和稀硫酸反应制氢气,为加快反应速率而不影响H2的品质,可向溶液中加适量Cu(NO3)2晶体.
分析 ①量筒感量是0.1mL;
②Fe(OH)3胶体与FeCl3溶液都能透过滤纸;
③试纸已经用蒸馏水湿润,稀释了待测溶液,且待测液酸碱性未知,无法确定;
④碱式滴定管下端的橡胶管能被酸性高锰酸钾腐蚀;
⑤锌和硝酸反应生成NO.
解答 解:①量筒感量是0.1mL,所以可以用量筒量取稀硫酸溶液8.0mL,故①正确;
②Fe(OH)3胶体与FeCl3溶液都能透过滤纸,所以不能用过滤的方法分离,应该用渗析的方法分离,故②错误;
③pH试纸用水润湿以后,再将待测液滴到pH试纸上,相当于把待测液给稀释了,如果待测液显酸性,则测出的pH偏大,如果待测液显碱性,则测出的pH偏小,如果待测液显中性,则pH不变,故③正确;
④碱式滴定管下端的橡胶管能被酸性高锰酸钾腐蚀,则应选酸式滴定管量取20.00mL 0.1000mol•L-1的KMnO4溶液,故④错误;
⑤锌和硝酸铜的酸性溶液反应生成NO,从而影响生成氢气的量,故⑤错误;
故选①③.
点评 本题考查了实验方案评价,涉及知识点较多,明确实验原理是解本题关键,注意⑤中隐含条件,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下列根据实验现象所得出的结论中,正确的是( )
| A. | 无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,则原溶液一定含有CO32- | |
| B. | 无色溶液中加入 AgNO3溶液,有白色沉淀生成,则原溶液一定含有Cl- | |
| C. | 无色溶液中加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝,则原溶液中一定含有NH4+ | |
| D. | 无色溶液中加入BaCl2溶液有白色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液一定含有SO42- |
3.下列各组物质与其用途的关系不正确的是( )
| A. | Na2O2:供氧剂 | B. | NaOH:治疗胃酸过多的一种药剂 | ||
| C. | 小苏打:发酵粉主要成分 | D. | 明矾:净水剂 |
20.下列实验中,所选试剂与装置均合理的是( )

| A. | 用饱和食盐水除去氯气中的氯化氢,选① | |
| B. | 分离溶液和胶体,选② | |
| C. | 用自来水制取蒸馏水,选③ | |
| D. | 用酒精提取碘水中的碘,选④ |
7.下列各组元素中,原子半径依次增大的是( )
| A. | Al、Si、P | B. | I、Br、Cl | C. | O、S、Na | D. | Mg、Ca、Ba |
17.关于氢键,下列说法正确的是( )
| A. | 氢键比范德华力强,所以它属于化学键 | |
| B. | 分子间形成的氢键使物质的熔点和沸点升高 | |
| C. | 由于NH3和H2O之间可形成分子间氢键,使氨在水中溶解度增大 | |
| D. | H2O是一种稳定的化合物,这是由于H2O之间形成氢键所致 |
4.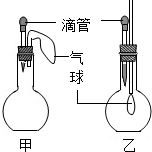 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大.(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大.(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )
 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大.(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大.(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )| A. | 甲:浓硫酸和木炭 乙:浓氨水和SO2 | |
| B. | 甲:双氧水和MnO2 乙:NaOH溶液和CO2 | |
| C. | 甲:苯酚和Na2CO3溶液 乙:NaOH溶液和Cl2 | |
| D. | 甲:浓硫酸和蔗糖(滴有几滴水) 乙:水和氨气 |
17.为了更好的解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源,以下做法不能提高燃料效率的是( )
| A. | 煤的汽化与液化 | B. | 液体燃料呈雾状喷出 | ||
| C. | 将煤压成煤球使用 | D. | 将煤粉燃烧 |