题目内容
【题目】工业上利用H2SiF6溶液制备BaF2 , 同时可得到副产品SiO2 , 其工艺如下: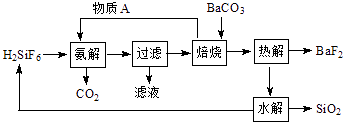
已知:焙烧过程的反应为(NH4)2SiF6+BaCO3 ![]() BaSiF6+2NH3↑+CO2↑+H2O↑
BaSiF6+2NH3↑+CO2↑+H2O↑
(1)焙烧的气体产物能恰好完全反应生成物质A,则A的化学式为 .
(2)氨解反应为放热反应,且反应能进行完全.该反应需降温冷却的原因为、 .
(3)热解的另一产物是含两种元素的气体,该气体水解的化学方程式是 .
(4)SiO2可用于制作 , 该物质在信息传输中具有重要应用.
(5)为保持该过程的持续循环,每生成1mol BaF2 , 理论上需补充原料H2SiF6mol.
【答案】
(1)(NH4)2CO3
(2)(NH4)2CO3受热易分解;减小(NH4)2SiF6晶体的溶解度
(3)3SiF4+2H2O=2H2SiF6+SiO2
(4)光导纤维
(5)![]()
【解析】解:利用H2SiF6溶液制备BaF2的流程为:H2SiF6溶液中加入碳酸铵进行氨解生成二氧化碳和(NH4)2SiF6晶体,由于(NH4)2CO3受热易分解同时也为了减小(NH4)2SiF6晶体的溶解度,氨解需降温冷却,过滤后将(NH4)2SiF6晶体与碳酸钡混合进行焙烧,生成BaSiF6和NH3、CO2、H2O,生成的NH3、CO2、H2O能恰好完全反应生成物质A,则A为碳酸铵,可进行循环利用,进行热解生成BaF2和另一产物是含两种元素的气体应为SiF4 , 水解可得H2SiF6和SiO2 , H2SiF6可循环利用,(1)根据上面的分析可知,A的化学式为(NH4)2CO3 , 所以答案是:(NH4)2CO3;(2)根据上面的分析可知,氨解反应需降温冷却的原因为(NH4)2CO3受热易分解、减小(NH4)2SiF6晶体的溶解度,
所以答案是:(NH4)2CO3受热易分解、减小(NH4)2SiF6晶体的溶解度;(3)热解的另一产物是含两种元素的气体为SiF4 , SiF4水解的化学方程式是 3SiF4+2H2O=2H2SiF6+SiO2 ,
所以答案是:3SiF4+2H2O=2H2SiF6+SiO2;(4)SiO2可用于制作光导纤维,
所以答案是:光导纤维;(5)根据方程式H2SiF6+(NH4)2CO3=(NH4)2SiF6+CO2+H2O、(NH4)2SiF6+BaCO3 ![]() BaSiF6+2NH3↑+CO2↑+H2O↑、BaSiF6+H2O=SiF4+BaF2、3SiF4+2H2O=2H2SiF6+SiO2可知,每1molH2SiF6参加反应可生成1mol BaF2同时又得到
BaSiF6+2NH3↑+CO2↑+H2O↑、BaSiF6+H2O=SiF4+BaF2、3SiF4+2H2O=2H2SiF6+SiO2可知,每1molH2SiF6参加反应可生成1mol BaF2同时又得到 ![]() mol的H2SiF6 , 所以为保持该过程的持续循环,理论上需补充原料H2SiF6
mol的H2SiF6 , 所以为保持该过程的持续循环,理论上需补充原料H2SiF6 ![]() mol,
mol,
所以答案是: ![]() .
.

【题目】为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是( )
序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
① | KNO3溶液 | KOH | 滴入稀HNO3,同时用pH试纸测定至溶液呈中性 |
② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
④ | NaCl | CaCO3 | 溶解、过滤、蒸发、结晶 |
A. ①②③ B. ②③④ C. ①③④ D. ①②③④
