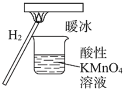
题目内容
【题目】2一氨-3—氯苯甲酸是白色晶体,其制备流程如下:
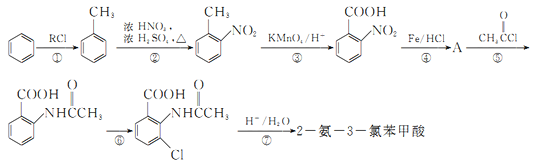
已知: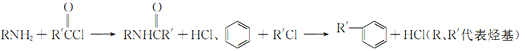
回答下列相关问题
(1)![]() 的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
(2)反应①中R代表的是_____________,反应②的反应类型为_____________。
(3)如果反应③中KMnO4的还原产物为MnSO4,请写出该反应的化学方程式_____________。
(4)A的结构简式为_____________,⑥的反应条件为_____________。
(5)符合下列条件的同分异构体的结构简式为_____________。
a.式量比![]() 大42的苯的同系物;
大42的苯的同系物;
b.与酸性KMnO4反应能生成二元羧酸
c.仅有3种等效氢
(6)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
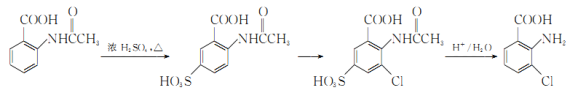
分析产率提高的原因是_____________。
【答案】甲苯 ![]() —CH3 取代反应
—CH3 取代反应 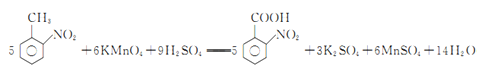
 Fe和Cl2
Fe和Cl2 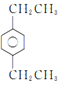 占位,减少5号位上H原子的取代
占位,减少5号位上H原子的取代
【解析】
由制备流程可知,苯与CH3Cl发生信息反应②生成甲苯,甲苯与浓硫酸和浓硝酸在加热条件下发生硝化反应生成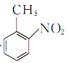 ,
, 发生氧化反应生成
发生氧化反应生成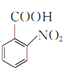 ,
, 与铁、盐酸发生还原反应生成A,则A为
与铁、盐酸发生还原反应生成A,则A为 ,
, 发生信息1反应生成
发生信息1反应生成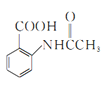 ,
, 在铁作催化剂的条件下,与氯气发生取代反应生成
在铁作催化剂的条件下,与氯气发生取代反应生成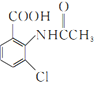 ,
, 在酸性条件下水解生成2一氨-3—氯苯甲酸。
在酸性条件下水解生成2一氨-3—氯苯甲酸。
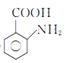
(1)![]() 的名称是甲苯;2-氨-3-氯苯甲酸的结构简式是
的名称是甲苯;2-氨-3-氯苯甲酸的结构简式是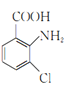 ,其含氮官能团为氨基,氨基的电子式为
,其含氮官能团为氨基,氨基的电子式为![]() ,故答案为:甲苯;
,故答案为:甲苯;![]() ;
;
(2)反应①为苯与CH3Cl反应生成甲苯,则R为—CH3;反应②为甲苯与浓硫酸和浓硝酸混酸在加热条件下发生硝化反应生成 ,故答案为:—CH3;
,故答案为:—CH3; ;
;
(3)反应③中,KMnO4与![]() 发生氧化还原反应,KMnO4被还原为MnSO4,
发生氧化还原反应,KMnO4被还原为MnSO4,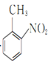 被氧化为
被氧化为![]() ,反应的化学方程式为
,反应的化学方程式为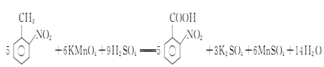 ,故答案为:
,故答案为: ;
;
(4) 与铁、盐酸发生还原反应生成A,则A为
与铁、盐酸发生还原反应生成A,则A为 ,反应⑥为
,反应⑥为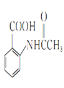 在铁作催化剂的条件下,与氯气发生取代反应生成
在铁作催化剂的条件下,与氯气发生取代反应生成 ,故答案为:
,故答案为: ;Fe和Cl2;
;Fe和Cl2;
(5)由a可知该物质比甲苯多3个—CH2—,由b可知该物质苯环上有2个取代基,其中取代基为—CH3和—CH2CH2CH3,在苯环上有邻、间、对3种同分异构体,取代基为—CH3和—CH(CH3)2,在苯环上有邻、间、对3种同分异构体,取代基为2个—CH2CH3,在苯环上有邻、间、对3种同分异构体,共9种,其中有3中等效氢的结构简式为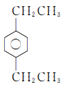 ,故答案为:
,故答案为: ;
;
(6)产率提高的原因是:占位可减少5号位上H原子的取代,减少副反应产物的生成,使得产率有了一定提高。故答案为:占位,减少5号位上H原子的取代。

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】PbCO3可用于油漆、陶瓷和玻璃等工业。由方铅矿(主要成分为PbS,含有杂质FeS等)和软锰矿(主要成分为MnO2)制备PbCO3的流程如下:
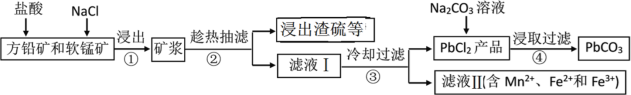
已知:PbCl2难溶于冷水和乙醇,易溶于热水;各物质的溶度积见表。试回答下列问题:
物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | PbCl2 | PbS | PbCO3 |
Ksp | 2×10-13 | 8.0×10-16 | 1×10-38 | 1.6×10-5 | 8.0×10-28 | 7.4×10-14 |
(1)PbCO3的名称是________。
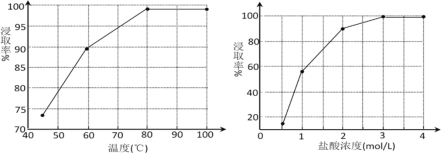
(2)步骤①中MnO2的作用是________,根据下图分析过程①的最佳反应条件是_________。
(3)步骤②趁热抽滤的原因是___________________。
(4)步骤③洗涤用的试剂是____________。
(5)将滤液Ⅱ先酸化,然后加入MnO2,反应的离子方程式为________;若反应后![]() ,进一步调节溶液的pH可分离出Fe3+和Mn2+,则调节溶液pH的范围为_________
,进一步调节溶液的pH可分离出Fe3+和Mn2+,则调节溶液pH的范围为_________![]() 时表示Fe3+已沉淀完全]。
时表示Fe3+已沉淀完全]。
(6)步骤④反应的离子方程式为______________。