题目内容
3.NaCl既是生活必需品,也是重要的化工原料.纯净的氯化钠可以用来制各氯气、氢气、盐酸、氢氧化钠、次氯酸钠,金属钠等物质.但海水中提取的NaCl中往往混有杂质.如图是模仿工业制备纯净的氯化钠溶液的工艺流程: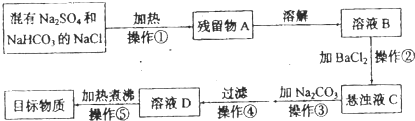
已知:下列物质的溶解度(25℃):
碳酸钡:1.409×10-3g;硫酸钡:2.448×10-4g
请回答下列问题:
(1)框图中“操作①”中“加热”的目的是使碳酸氢钠分解转化为碳酸钠,完成该操作所需要的主要硅酸盐实验仪器除酒精灯、玻璃棒外,还有坩埚.
(2)写出操作②中出现沉淀的离子方程式:Ba2++CO32-=BaCO3↓、Ba2++SO42-=BaSO4↓.
加入过量的BaCl2后,溶液中离子的浓度大小关系为SO42-<CO32-(选填“>”、“=”或“<”).
(3)进行操作②后,如何判断SO42-已经除尽?用洁净的试管取少量上层清液,向试管中滴加酸化的氯化钡溶液,若无沉淀产生,则说明硫酸根离子已经除尽.
(4)“目标物质”应该是纯净的NaCl溶液,但根据上述方法制备的“目标物质”中含有杂质碳酸钠,应该如何改进上述制备工艺:在操作④之后加入适量的盐酸并测定pH值,除去溶液中碳酸根离子.
分析 混有硫酸钠和碳酸氢钠的氯化钠加热后,碳酸氢钠受热分解,得残留物A中含有硫酸钠、碳酸钠、氯化钠,溶解后得混合溶液B,B中加入氯化钡溶液生成硫酸钡沉淀和碳酸钡沉淀,充分搅拌得悬浊液C,在C中加碳酸钠除去多余的氯化钡,过滤得溶液D主要含有氯化钠另有部分碳酸钠,经蒸发结晶可得氯化钠固体,
(1)加热可使碳酸氢钠分解;灼烧固体应在坩埚中进行;
(2)碳酸钠、硫酸钠与氯化钡生成碳酸钡、硫酸钡沉淀,因为碳酸钡比硫酸钡易溶,所以碳酸钡可以转化成硫酸钡,据此答题;
(3)判断SO42-已经除尽,可以在沉淀后的上层清液中检验硫酸根离子,可以用氯化钡;
(4)根据上面的分析可知,目标物质中含有碳酸钠,可以用盐酸除去碳酸钠;
解答 解:混有硫酸钠和碳酸氢钠的氯化钠加热后,碳酸氢钠受热分解,得残留物A中含有硫酸钠、碳酸钠、氯化钠,溶解后得混合溶液B,B中加入氯化钡溶液生成硫酸钡沉淀和碳酸钡沉淀,充分搅拌得悬浊液C,在C中加碳酸钠除去多余的氯化钡,过滤得溶液D主要含有氯化钠另有部分碳酸钠,经蒸发结晶可得氯化钠固体,
(1)加热可使碳酸氢钠分解转化为碳酸钠,灼烧固体应在坩埚中进行,
故答案为:使碳酸氢钠分解转化为碳酸钠;坩埚;
(2)碳酸钠、硫酸钠与氯化钡生成碳酸钡、硫酸钡沉淀,反应的离子方程式为Ba2++CO32-=BaCO3↓、Ba2++SO42-=BaSO4↓,因为碳酸钡比硫酸钡易溶,所以碳酸钡可以转化成硫酸钡,所以溶液中离子的浓度大小关系为SO42-<CO32-,
故答案为:Ba2++CO32-=BaCO3↓、Ba2++SO42-=BaSO4↓;<;
(3)判断溶液B中SO42-已经除尽的方法为用洁净的试管取少量上层清液,向试管中滴加酸化的氯化钡溶液,若无沉淀产生,则说明硫酸根离子已经除尽,
故答案为:用洁净的试管取少量上层清液,向试管中滴加酸化的氯化钡溶液,若无沉淀产生,则说明硫酸根离子已经除尽;
(4)根据上面的分析可知,目标物质中含有碳酸钠,改进的方法是在操作④之后加入适量的盐酸并测定pH值,除去溶液中碳酸根离子,
故答案为:碳酸钠;在操作④之后加入适量的盐酸并测定pH值,除去溶液中碳酸根离子.
点评 本题考查了粗盐的提纯、溶液的配制级有关化学方程式的计算等相关知识,侧重基础知识的灵活应用,难度不大.

| A. | 某些馆的外壳使用非晶硅薄膜,以充分利用太阳能 | |
| B. | 世博会期间,利用可降解的“主米塑料”替代一次性饭盒,可防止产生白色污染 | |
| C. | 世博会中国馆“东方之冠”使用的钢筋混凝土属于高分子化合物 | |
| D. | 世博停车场安装催化光解设施,可将汽车尾气中的CO和NO 转化为无毒气体CO2和N2 |
| A. | Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物 | |
| B. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 | |
| C. | 与相同浓度的酸反应的速率:Na2CO3<NaHCO3 | |
| D. | Na着火时可用泡沫灭火器灭火 |
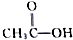 、
、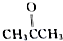 及
及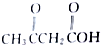 .根据上述事实推测A可能的构造式.
.根据上述事实推测A可能的构造式.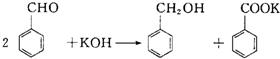
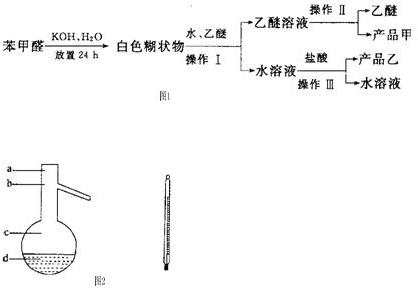
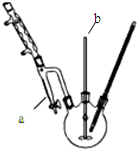 塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂.反应原理为:
塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂.反应原理为: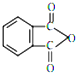 +2CH3CH2CH2CH2OH→
+2CH3CH2CH2CH2OH→ +H2O
+H2O +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$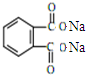 +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.