题目内容
下列图示与对应的叙述相符的是( )
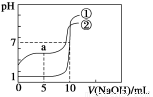
A.图Ⅰ表示常温下盐酸滴加到0.1 mol·L-1某碱溶液中得到的滴定曲线,由图Ⅰ可知二者恰好中和时,所得溶液的pH>7
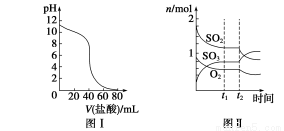
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度
2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度
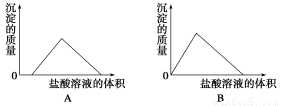
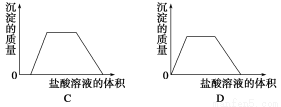
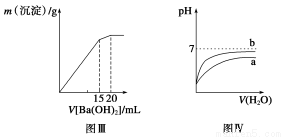
C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时,沉淀全部是BaSO4
D.图Ⅳ表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸
C
【解析】A项,由图 Ⅰ 知碱是弱碱,恰好中和时pH<7,错误;B项,根据t2时曲线的变化情况,改变的应是降低温度,错误;C项,根据KAl(SO4)2+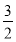 Ba(OH)2=Al(OH)3↓+
Ba(OH)2=Al(OH)3↓+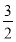 BaSO4↓+
BaSO4↓+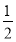 K2SO4,再加入
K2SO4,再加入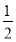 mol Ba(OH)2时,发生Al(OH)3+OH-=AlO2-+2H2O,全部溶解,
mol Ba(OH)2时,发生Al(OH)3+OH-=AlO2-+2H2O,全部溶解,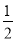 K2SO4+
K2SO4+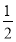 Ba(OH)2=KOH+
Ba(OH)2=KOH+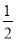 BaSO4↓,又增加
BaSO4↓,又增加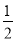 mol的BaSO4,正确;D项,pH相同,当加水稀释相同倍数,CH3COOH的pH变化小,a对应的是CH3COOH,错误。
mol的BaSO4,正确;D项,pH相同,当加水稀释相同倍数,CH3COOH的pH变化小,a对应的是CH3COOH,错误。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1
2XY3(g) ΔH=-92.6 kJ·mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化 | ||
X2 | Y2 | XY3 | ||
① | 1 | 3 | 0 | 放热:23.15 kJ |
② | 0.6 | 1.8 | 0.8 | Q(Q>0) |
下列叙述不正确的是( )
A.容器①、②中反应的平衡常数相等
B.容器②中反应达到平衡时放出的热量为Q
C.达到平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
D.若容器①的体积为0.20 L,则达平衡时放出的热量大于23.15 kJ