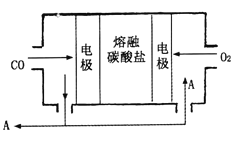
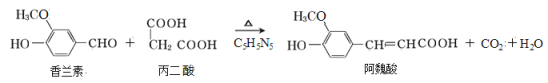题目内容
【题目】常温下,下图表示向10mLpH=3的A溶液中加水稀释到V1mL溶液pH的变化。下列说法中正确的是( )
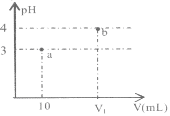
A.若V1=100,则稀释前A的浓度一定是0.001mol/L
B.若A为NH4Cl和HCl的混合溶液,则V1一定大于100
C.a点水的电离程度一定小于b点
D.若A为NH4Cl和NH3·H2O的混合溶液,则溶液中c(NH4+)>c(Cl-)>c(H+)>c(OH-)
【答案】B
【解析】
试题分析:稀释10倍,PH增大1,说明A是强酸, 若A是二元酸,浓度一定是0.0005mol/L,故A错误;NH4Cl水解呈酸性,稀释10倍,PH<4,故B正确;若A是盐溶液,.a点水的电离程度一定大于b点,故C错误;若A为NH4Cl和NH3·H2O的混合溶液,则溶液中c(Cl-)>c(NH4+) >c(H+)>c(OH-),故D错误。

 阅读快车系列答案
阅读快车系列答案【题目】乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体。某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答。
【观察与思考】
(1)乙醇分子的核磁共振氢谱有 个吸收峰。
【活动与探究】
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象。请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满)。
实验现象 | 结 论 | |
① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
② |
(3)乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次。则此时乙醇发生反应的化学方程式为(生成乙醛)____________________________________。欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为__________________________________________。
【交流与讨论】
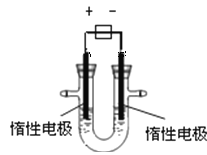
(4)丙同学向一支试管中加入3 mL 乙醇,然后边摇动试管边慢慢加入2 mL浓硫酸和2 mL冰醋酸,按右图所示连接好装置,请指出该装置的主要错误是 。假如乙醇分子中的氧原子为18O原子,则发生此反应后1 8O原子将出现在生成物 中(填字母)。
A.水 B.乙酸乙酯 C.水和乙酸乙酯