题目内容
【题目】制取氨气并完成与氨气性相关的实验(图中夹持装置均已略去)。
(1)写出实验室制取氨气的化学方程式________________。
(2)要得到干燥的氨气可选用__________做干燥剂(填序号)
A.无水 CaCl2 B.浓硫酸 C.P2O5 D.碱石灰
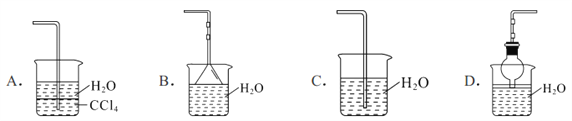
(3)已知氨气难溶于有机溶剂 CCl4。下列装置中可以做 NH3的尾气吸收装置的有______。
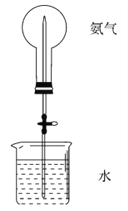
(4)如果只提供如图的装置,请说明引发喷泉的方法___________。
【答案】 Ca(OH)2 + 2NH4Cl![]() CaCl2 + 2NH3↑ + 2H2O D A、B、D 打开止水夹,用手或热毛巾捂热烧瓶
CaCl2 + 2NH3↑ + 2H2O D A、B、D 打开止水夹,用手或热毛巾捂热烧瓶
【解析】(1)实验室制取氨气的化学方程式为Ca(OH)2 + 2NH4Cl![]() CaCl2 + 2NH3↑ + 2H2O。(2)氨气是碱性气体,可以用碱石灰干燥,不能用浓硫酸和酸性氧化物P2O5干燥。又因为氨气能与氯化钙反应,所以也不能用氯化钙干燥,答案选D。(3)A.氨气不溶于四氯化碳,该装置可以防止倒吸,可用于吸收氨气,A正确;B.使用倒置的漏斗,可以防止倒吸,可用于吸收氨气尾气,B正确;C.氨气极易溶于水,不能直接将导管插入水中,否则容易发生倒吸,C错误;D.球形漏斗可以防止倒吸,可用于吸收氨气尾气,D正确;答案选ABD。(4)加热时烧瓶内压强增大,气体体积膨胀,当氨气与水接触时,因氨气极易溶于水而导致烧瓶内压强迅速减小而形成喷泉,因此正确的操作为打开止水夹,用手或热毛巾捂热烧瓶。
CaCl2 + 2NH3↑ + 2H2O。(2)氨气是碱性气体,可以用碱石灰干燥,不能用浓硫酸和酸性氧化物P2O5干燥。又因为氨气能与氯化钙反应,所以也不能用氯化钙干燥,答案选D。(3)A.氨气不溶于四氯化碳,该装置可以防止倒吸,可用于吸收氨气,A正确;B.使用倒置的漏斗,可以防止倒吸,可用于吸收氨气尾气,B正确;C.氨气极易溶于水,不能直接将导管插入水中,否则容易发生倒吸,C错误;D.球形漏斗可以防止倒吸,可用于吸收氨气尾气,D正确;答案选ABD。(4)加热时烧瓶内压强增大,气体体积膨胀,当氨气与水接触时,因氨气极易溶于水而导致烧瓶内压强迅速减小而形成喷泉,因此正确的操作为打开止水夹,用手或热毛巾捂热烧瓶。

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2): 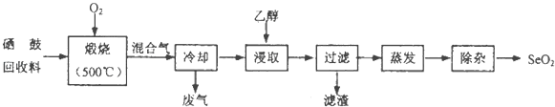
部分物质的物理性质如表:
物质 | 熔点 | 沸点 | 溶解度 |
SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水和乙醇 |
TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水,不溶于乙醇 |
回答下列问题:
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为;H2Se的热稳定性比H2S的热稳定性(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是 . 蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是 .
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式 .
(4)已知H2SeO3的电离常数K1=3.5×10﹣3、K2=5.0×10﹣8 , 回答下列问题:
①Na2SeO3溶液呈性,原因是(用离子方程式表示);
②在Na2SeO3溶液中,下列关系式正确的是:
A.c(Na+)+c(H+)=c(SeO32﹣)+c(HSeO3﹣)+c(OH﹣)
B.2c(Na+)=c(SeO32﹣)+c(HSeO3﹣)+c(H2SeO3)
C.c(Na+)=2c(SeO32﹣)+2c(HSeO3﹣)+2c(H2SeO3)
D.c(OH﹣)=c(H+)+c(HSeO3﹣)+c(H2SeO3)