题目内容
13.下列各组物质,都能使溴水褪色的是( )| A. | 苯酚溶液、氨水、氯水 | B. | AgNO3溶液、KBr溶液、K2SO4溶液 | ||
| C. | 苯乙烯、己烯、电石气 | D. | KI溶液、H2S溶液、NaOH溶液 |
分析 能使溴水褪色的有机物中含有醛基、碳碳饱和键键或酚羟基,溴具有强氧化性,能和还原性物质发生氧化还原反应,据此分析解答.
解答 解:A.氯气和溴都具有强氧化性,二者不发生反应,所以不能使溴水褪色,故A错误;
B.溴化钾和溴不反应、硫酸钾和溴不反应,所以KBr溶液、K2SO4溶液不能使溴水褪色,故B错误;
C.苯乙烯、己烯、电石气中都含有碳碳不饱和键,所以都能和溴发生加成反应而使溴水褪色,故C正确;
D.溴和碘化钾发生置换反应生成碘,单质溶液由橙色变为紫色,故D错误;
故选C.
点评 本题考查有机物的结构和性质,明确官能团及其性质关系是解本题关键,知道溴具有强氧化性,能氧化还原性物质,题目难度不大.

练习册系列答案
相关题目
8. 研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.
研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.
(1)C、Si、N元素的电负性由大到小的顺序是N>C>Si.
(2)A、B均为短周期金属元素.依据下表数据,写出B原子的电子排布式:1s22s22p63s2.
(3)依据第2周期元素第一电离能的变化规律,参照图中B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置.
(4)基态铜原子的核外电子排布式为1s22s22p63s23p63d104s1.
(5)基态Si原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9、电子数为4.
 研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.
研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.(1)C、Si、N元素的电负性由大到小的顺序是N>C>Si.
(2)A、B均为短周期金属元素.依据下表数据,写出B原子的电子排布式:1s22s22p63s2.
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(4)基态铜原子的核外电子排布式为1s22s22p63s23p63d104s1.
(5)基态Si原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9、电子数为4.
4.下列关于氢元素的叙述中,错误的是( )
| A. | 自然界中有11H、12H、13H三种氢的同位素,它们的化学性质不相同 | |
| B. | ${\;}_{1}^{1}$H失去1个电子后,变成1个质子 | |
| C. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H是三种不同的原子 | |
| D. | 11H、21H、31H在化学反应中容易失去一个电子而显+1价 |
8.下列说法不正确的是( )
| A. | 烃是指仅含碳和氢两种元素的有机物 | |
| B. | 含碳化合物都属有机物 | |
| C. | 分子里含有苯环的碳氢化合物属于芳香烃 | |
| D. | 通常所说的“白色污染”是指聚乙烯等白色塑料垃圾 |
18.氢元素与其它元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
| A. | 一个D2O分子所含的中子数为8 | |
| B. | NH3的结构式为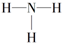 | |
| C. | HCl的电子式为H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| D. | 热稳定性:HCl>HF |
5.在标准状况下,相同质量的下列气体中体积最大的是( )
| A. | NO | B. | CO2 | C. | N2 | D. | O2 |
2.利用下列反应不能制得括号中纯净物质的是( )
| A. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| B. | 等物质的量的氯气与乙烷在光照下反应(氯乙烷) | |
| C. | 乙烯与水加成(乙醇) | |
| D. | 乙烯与氯化氢在一定条件下反应(氯乙烯) |
 工业合成氨是利用氮气和氢气在一定条件下反应生成的.氨是重要的工业原料.请回答下列问题:
工业合成氨是利用氮气和氢气在一定条件下反应生成的.氨是重要的工业原料.请回答下列问题: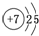 ;
; ;指出分子中化学键是共价键(填‘离子键’或‘共价键’).
;指出分子中化学键是共价键(填‘离子键’或‘共价键’). ;C 单质在高温下与B单质充分反应所得化合物的电子式为
;C 单质在高温下与B单质充分反应所得化合物的电子式为
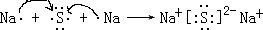 .
.