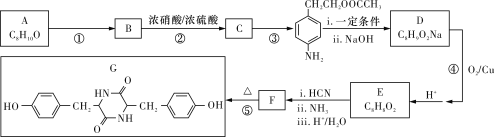
��Ŀ����
����Ŀ��������������ˮ�������ᣬ���������Լ���ҽ�÷���������������������һ���Ʊ�
�������Ƶ�ʵ�鷽�����ش��������⣺
��һ��̼��Ƶ��Ʊ�

���������백ˮ��Ŀ����________________��С����е�������ʹ������������������__________________��
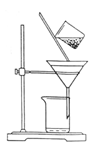
(2)��ͼ��ijѧ���Ĺ��˲���ʾ��ͼ����������淶����_________�����ţ���
a��©��ĩ�˾���δ�����ձ���
b����������������
c������ֽʪ��ʹ�����©����
d����ֽ��Ե�߳�©��
e���ò�������©������������Լӿ�����ٶ�
(��)�������Ƶ��Ʊ�
![]()
(3)�������ľ������Ϊ��μ���ϡ���ᣬ����Һ���д����������壬��ʱ��Һ��_______�ԣ���������������������������������Һ��У����ȹ��ˡ�����Һ��е�������______________��
(4)�������з�Ӧ�Ļ�ѧ����ʽΪ____________________��
(5)�����˵õ��İ�ɫ�ᾧ����ʹ������ˮ���Ҵ�ϴ�ӣ�ʹ���Ҵ�ϴ�ӵ�Ŀ����___________��
(6)�Ʊ��������Ƶ���һ�ַ����ǣ���ʯ��ʯ���պ�ֱ�Ӽ���˫��ˮ��Ӧ�����˺�ɵõ��������Ʋ�Ʒ���ù��շ������ŵ���______________����Ʒ��ȱ����_______________��
���𰸡�(1)������ҺpHʹFe(OH)3���������˷���
(2)ade (3)������ȥ��Һ���ܽ��CO2
(4)CaCl2��2NH3��H2O��H2O2=CaO2����2NH4Cl��2H2O��
CaCl2��2NH3��H2O��H2O2��6H2O=CaO2��8H2O����2NH4Cl
(5)ȥ���ᾧ����ˮ��(6)���ռ��������㣻���Ƚϵ�
��������
�����������1��ʯ��ʯ�к��������������˫��ˮ��Ŀ���ǽ�������������Ϊ�����ӣ��ټӰ�ˮ������pHʹ������ת��Ϊ����������ȥ��С����е�������ʹ�����������������ڽ������Ĺ��˲�������Ϊ��������ҺpHʹFe(OH)3��������Ϊ��������ҺpHʹFe(OH)3���������˷�������2�����˲����в��淶���ǣ�a��©��ĩ�˾���δ�����ձ��ڣ������Һ��ɽ���d����ֽ��Ե�߳�©����������ֽŪ�ƣ�e���ò�������©������������Լӿ�����ٶȣ�������ֽ���ƣ���Ϊ��ade����3���������ľ������Ϊ��μ���ϡ���ᣬ����Һ���д����������壬��Һ�е��������Ȼ��ƺ��ܽ������������̼����ʱ��Һ�����ԣ���е�Ŀ����Ϊ�˳�ȥʣ���û�лӷ����CO2����Ϊ��������ȥ��Һ���ܽ��CO2����4���������з�Ӧ�Ļ�ѧ����ʽΪCaCl2 �� 2NH3��H2O �� H2O2 = CaO2�� �� 2NH4Cl �� 2H2O��CaCl2 �� 2NH3��H2O �� H2O2 �� 6H2O = CaO2��8H2O�� �� 2NH4Cl����Ϊ��CaCl2 �� 2NH3��H2O �� H2O2 = CaO2�� �� 2NH4Cl �� 2H2O��CaCl2 �� 2NH3��H2O �� H2O2 �� 6H2O = CaO2��8H2O�� �� 2NH4Cl����5�����Ҵ�ϴ����Ҫ�������Ҵ����лӷ��ԣ��������Ҵ���ȥ��������ˮ�֣���Ϊ��ȥ���ᾧ����ˮ�֣���6����ʯ��ʯ���պ�ֱ�Ӽ���˫��ˮ��Ӧ�����˺�ɵõ��������Ʋ�Ʒ��ù�����������ŵ��ǹ��ռ��������㣬���������Ʊ��Ĺ��������е����ʺܶ࣬���Ƚϵͣ���Ϊ�����ռ��������㣻���Ƚϵ͡�

 Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д� ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д�����Ŀ����X����ͨ��BaCl2��Һ��δ���������ɣ�Ȼ��ͨ��Y���壬�г������ɣ�X��Y�����ܵ���
ѡ�� | A�� | B�� | C�� | D�� |
X | SO2 | CO2 | CO2 | SO2 |
Y | Cl2 | Cl2 | NH3 | H2S |