题目内容
【题目】在实验室中,下列除去杂质的方法不正确的是
A.溴苯中混有溴,加稀氢氧化钠反复洗涤、分液
B.乙烯中混有SO2、CO2,将其通入NaOH溶液洗气
C.除去CO2中少量的SO2:气体通过盛饱和碳酸氢钠溶液的洗气瓶
D.乙烷中混有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷
【答案】D
【解析】
试题分析:A.溴能稀氢氧化钠溶液反应,溴苯不溶于氢氧化钠溶液,分层后分液即可,正确;B. SO2、CO2是酸性氧化物,能够溶于NaOH溶液,乙烯不溶,正确;C. SO2溶于水生成亚硫酸,能够与饱和碳酸氢钠溶液反应放出二氧化碳,而二氧化碳在饱和碳酸氢钠溶液中溶解度很小,正确;D.会混入新杂质氢气,错误;故选D。

练习册系列答案
相关题目
【题目】已知:Fe(OH)3和Al(OH)3沉淀的生成与溶解的pH如下表。
氢氧化物 | 溶液pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | —— | —— |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如下图所示。以下推断错误的是
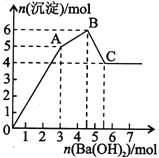
A.AB段可能发生的反应:2Ba2++3OH-+2SO42-+Al3+=2BaSO4↓+Al(OH)3↓
B.C点对应的沉淀:Fe(OH)3和BaSO4
C.OA段可能发生的反应:3Ba2++6OH-+3SO42-+Al3++Fe3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓
D.据图计算原溶液中:c(Cl-)=c(SO42-)