题目内容
4.可逆反应H2(g)+I2(g)?2HI(g)达到平衡的标志是( )| A. | H2、I2、HI的浓度相等 | B. | H2、I2、HI的浓度之比为1:1:2 | ||
| C. | 混合气体的平均相对分子质量不变 | D. | 混合气体的颜色不再改变 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、H2、I2、HI的浓度不变,而不是相等,故A错误;
B、当体系达平衡状态时,H2、I2、HI的浓度之比可能为1:1:2,也可能不是,与各物质的初始浓度及转化率有关,故B错误;
C、气体两边的计量相等,所以混合气体的平均相对分子质量始终不变,故C错误;
D、混合气体的颜色不再改变,说明碘蒸气的浓度不变,达化学平衡状态,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.化学知识在生产、生活中有着广泛的应用.下列说法中正确的是( )
| A. | 铅蓄电池属于二次电池 | |
| B. | 氢氟酸可用于蚀刻玻璃是因为其具有强酸性 | |
| C. | 为了防止食品受潮,常在食品包装袋中放入活性铁粉 | |
| D. | 用于制光缆的光导纤维是新型有机高分子材料 |
15.合理开发和利用海水资源是世界各国研究的课题.下列对于海水利用的认识错误的是( )
| A. | 海水中蕴藏有丰富的资源,人类可以大量开发,以弥补资源的短缺 | |
| B. | 海水可以成为廉价的资源基地,但要合理开发,综合利用 | |
| C. | 可以用太阳能电解海水以获取氢能源 | |
| D. | 人类在利用海水时要兼顾海洋生物和海洋生态平衡 |
12.据最新报道,放射性同位素钬${\;}_{67}^{166}$Ho可有效地治疗肝癌.该同位素原子内中子数为( )
| A. | 99 | B. | 67 | C. | 32 | D. | 166 |
19.用惰性电极电解下列足量的溶液,一段时间后,再加入一定量的另一物质(括号内)后,溶液能与原来溶液浓度一样的是( )
| A. | CuCl2(CuCl2溶液) | B. | AgNO3(Ag2O) | C. | NaCl(HCl溶液) | D. | CuSO4(Cu(OH)2) |
9.将一定量的Fe、FeO和Fe2O3混合物投入到150 mL 2 mol•L-1的HNO3溶液中,恰好使混合物完全溶解,并生成1.12L NO气体(标准状况),在所得溶液中加入KSCN溶液,无血红色出现.若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
| A. | 7 g | B. | 14 g | C. | 28 g | D. | 无法计算 |
16.下列推断正确的是( )
| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | Na2CO3、NaHCO3都是盐,都能与CaCl2溶液反应 | |
| C. | CO、NO都是大气污染气体,在空气中都能稳定存在 | |
| D. | Fe和Al都是金属,都不能与碱溶液反应 |
14.下列化学表述正确的是( )
| A. | 氯化钠的晶体模型: | |
| B. | 铍原子最外层的电子云图: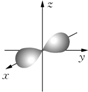 | |
| C. | 次氯酸的结构式:H-O-Cl | |
| D. | CH3CHOHCH(CH3)2名称:2-3-二甲基丙醇 |