题目内容
已知:2Al (s)+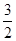 O2(g)=== Al2O3(s) △H=" -1" 644.3 kJ? mol-1
O2(g)=== Al2O3(s) △H=" -1" 644.3 kJ? mol-1
2Fe (s) +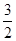 O2(g)=== Fe2O3(s) △H=" -815.88" kJ? mol-1
O2(g)=== Fe2O3(s) △H=" -815.88" kJ? mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式___________________________。
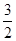 O2(g)=== Al2O3(s) △H=" -1" 644.3 kJ? mol-1
O2(g)=== Al2O3(s) △H=" -1" 644.3 kJ? mol-12Fe (s) +
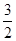 O2(g)=== Fe2O3(s) △H=" -815.88" kJ? mol-1
O2(g)=== Fe2O3(s) △H=" -815.88" kJ? mol-1试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式___________________________。
2Al(s)+Fe2O3(s)=Al2O3(s)+2Fe(s) △H=-828.42kJ·mol-1
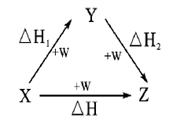
考查盖斯定律的应用。根据盖斯定律可知,①-②即得到
2Al(s)+Fe2O3(s)=Al2O3(s)+2Fe(s) ,所以反应热△H=―1 644.3 kJ? mol-1+815.88 kJ? mol-1=-828.42kJ·mol-1。
2Al(s)+Fe2O3(s)=Al2O3(s)+2Fe(s) ,所以反应热△H=―1 644.3 kJ? mol-1+815.88 kJ? mol-1=-828.42kJ·mol-1。

练习册系列答案
相关题目
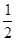 CH4(g)+O2(g)=
CH4(g)+O2(g)= 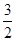 O2(g)=CO(g)+2H2O(1); ?H=-607.3kJ·mol-1
O2(g)=CO(g)+2H2O(1); ?H=-607.3kJ·mol-1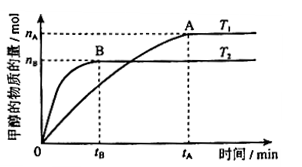
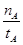 mol·L-1·min-1
mol·L-1·min-1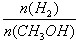 增大
增大 2CO2(g)反应过程的能量变化如图所示。已知1 mol CO (g)氧化为1 mol CO2 (g)的ΔH =-283 kJ/mol。请回答下列问题:
2CO2(g)反应过程的能量变化如图所示。已知1 mol CO (g)氧化为1 mol CO2 (g)的ΔH =-283 kJ/mol。请回答下列问题:
 2SO3(g);△H=-Q kJ·mol-1(Q>0),向密闭恒容容器甲中通入l mol SO2和0.5 mol O2,向另一密闭恒容容器乙中通入2 mol SO2和1 mol O2,起始时两容器中气体的温度和压强相同,反应达到平衡时,两容器中气体的温度和压强仍相同,此时甲中放出的热量为Ql kJ,乙中放出的热量为Q2 kJ。则下列关系式正确的是 ( )
2SO3(g);△H=-Q kJ·mol-1(Q>0),向密闭恒容容器甲中通入l mol SO2和0.5 mol O2,向另一密闭恒容容器乙中通入2 mol SO2和1 mol O2,起始时两容器中气体的温度和压强相同,反应达到平衡时,两容器中气体的温度和压强仍相同,此时甲中放出的热量为Ql kJ,乙中放出的热量为Q2 kJ。则下列关系式正确的是 ( )