题目内容
【题目】已知硫酸、氨水的密度与所加水量的关系如图所示:

现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶液 | 溶质的物质的量浓度 | 溶液的密度/g·cm-3 |
硫酸 | 4 mol·L-1 | ρ1 |
2 mol·L-1 | ρ2 | |
氨水 | 4 mol·L-1 | ρ3 |
2 mol·L-1 | ρ4 |
⑴ ρ1、ρ2、ρ3、ρ4由大到小的顺序为:________。
⑵ 表中2 mol·L-1氨水的质量分数为:________。
⑶ 将4 mol·L-1的氨水与2 mol·L-1的氨水等质量混合,所得氨水的物质的量浓度是_____(填序号)。
A.>3 mol·L-1 B.=3 mol·L-1 C.<3 mol·L-1 D.无法判断
⑷ 将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是______(填序号)。
A.>15% B.=15% C.<15% D.无法判断
⑸ 100g浓度为4 mol·L-1的硫酸溶液与_________mL水混合,能使硫酸的物质的量浓度减小到2 mol·L-1。
【答案】 ρ1>ρ2>ρ4>ρ3 (3.4/ρ4) % A A (200ρ2-100ρ1)/ ρ1
【解析】(1)硫酸的密度大于水的密度,氨水的密度小于水的密度,所以ρ1、ρ2>ρ4、ρ3,硫酸的密度大于水的密度,浓度越大,密度越大,ρ1>ρ2,氨水的密度小于水的密度,浓度越大,密度越小,ρ4>ρ3,因此大小顺序为ρ1>ρ2>ρ4>ρ3;(2)表中2molL-1氨水的密度是ρ4,根据公式c=1000ρw/M得出质量分数为:w=3.4/ρ4 %;(3)由图可知,氨水的浓度越大密度越小,将4molL-1的氨水与2molL-1的氨水等质量混合,所得氨水的物质的量浓度要比3molL-1大,答案选A;(4)硫酸的密度大于水的密度,将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数>(20%+10%)/2,即混合后质量分数大于15%,答案选A;(5)100g浓度为4molL-1的硫酸溶液中溶质的物质的量是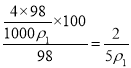 ,设加入水的体积是VmL,能使硫酸的物质的量浓度减小到2molL-1,则
,设加入水的体积是VmL,能使硫酸的物质的量浓度减小到2molL-1,则![]() ,解得V=(200ρ2100ρ1)/ρ1mL。
,解得V=(200ρ2100ρ1)/ρ1mL。

【题目】根据下列实验或实验操作和现象,所得结论正确的是
实验或实验操作 | 现象 | 实验结论 | |
A | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
C |
| 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
D |
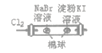
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
A. A B. B C. C D. D