题目内容
【题目】下列各组溶液,当后一种溶液逐滴加入到一定量的前一种溶液中并稍过量,其溶液的导电性(I表示导电能力)与后一种溶液的质量(m)的函数关系符合下图的是
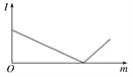
A. 澄清石灰水、碳酸钠溶液
B. 硝酸银溶液、氯化钠溶液
C. 盐酸、氢氧化钠溶液
D. 稀硫酸、氢氧化钡溶液
【答案】D
【解析】
溶液的导电性与单位体积内离子的数目、离子所带电荷多少有关,单位体积内离子数目越多,导电性越强;离子所带电荷越多,导电性越强(如两个氯离子和一个硫酸根离子导电性相当)进行分析作答。
A. 澄清石灰水和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,溶液中的离子数目没有明显减少,所以导电性不会明显减弱至接近零,故A项错误;
B. 硝酸银溶液和氯化钠溶液反应生成氯化银沉淀和硝酸钠,溶液中的离子数目没有明显减少,所以导电性不会明显减弱至接近零,故B项错误;
C. 盐酸和氢氧化钠溶液反应生成氯化钠和水,溶液中的离子数目没有明显减少,所以导电性不会明显减弱至接近零,故C项错误;
D. 稀硫酸和氢氧化钡溶液反应硫酸钡沉淀和水,水难电离,硫酸钡难溶于水,所以溶液的导电性不断减弱,当氢氧化钡溶液和硫酸恰好反应,导电性最弱接近零,当氢氧化钡溶液过量时,溶液中的离子数目又增多,导电性增强,符合题意,故D项正确;
答案选D。

练习册系列答案
相关题目