题目内容
【题目】半导体材料磷化硼(BP)可由BBr3和PBr3在高温下合成。回答下列问题:
(1)在现代化学中,常利用______________(填“原子光谱”或“分子光谱”) 上的特征谱线来鉴定元素,称为光谱分析。
(2)基态P原子的价电子排布式为_______,同周期中第一电离能比P小的元素有_______种。
(3)在水中的溶解度BBr3_________PBr3(填“>”或“<”),原因是____________________。
(4)一定温度下PBr5能形成阴、阳离子个数比为1:1的导电熔体,阴阳离子均带一个电位电荷,经测定其中P-Br键键长均相等。写出该导电熔体中阳离子的电子式:_____________,其中P原子的杂化轨道类型是_____________________。
(5)已知磷化硼晶体中P原子作面心立方最密堆积,若某个P的原子坐标为(0,0,0),则晶胞中其余P原子的坐标为______________ (写出一个即可),B原子填入四面体空隙中,B的原子坐标分别为(![]() ,
,![]() ,
,![]() )、(
)、(![]() ,
,![]() ,
,![]() )、(
)、(![]() ,
,![]() ,
,![]() )、(
)、(![]() ,
,![]() ,
,![]() ),相邻P原子和B原子核间距为dcm,则该晶体中每个B原子周围有______个B原子与它距离最近,晶体密度为________g·cm-3 (NA表示阿 伏加德罗常数的值)。
),相邻P原子和B原子核间距为dcm,则该晶体中每个B原子周围有______个B原子与它距离最近,晶体密度为________g·cm-3 (NA表示阿 伏加德罗常数的值)。
【答案】 原子光谱 3s2 3p3 5 < BBr3为非极性分子而PBr3为极性分子 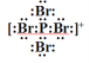 sp3 (
sp3 (![]() ,
,![]() ,0)[或(0,
,0)[或(0,![]() ,
,![]() )(
)(![]() ,0,
,0,![]() )] 12
)] 12 ![]()
【解析】考查物质结构与性质的综合运用,(1)光谱分析是利用原子光谱上的特征谱线进行元素的鉴定;(2)P位于VA族,价电子为最外层电子,即价电子排布式为3s23p3;同周期从左向右第一电离能增大,但IIA>IIIA,VA>VIA,同周期中第一电离能比P小的元素有5种;(3)BBr3空间构型为平面正三角形,属于非极性分子,PBr3空间构型为三角锥形,属于极性分子,水为极性分子,根据相似相溶,BBr3的溶解性小于PBr3;(4)P-Br键键长均相等,空间构型一个是正四面体,一个是正六面体,阳离子是PBr4+,阴离子是PBr6-,即阳离子的电子式为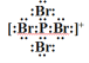 ,P有4个σ键,无孤电子对,价层电子对数为4,杂化类型为sp3;(5)P原子为面心立方最密堆积,位于顶点和面心,若某一个P的坐标是(0,0,0),其余P的坐标可以是 (
,P有4个σ键,无孤电子对,价层电子对数为4,杂化类型为sp3;(5)P原子为面心立方最密堆积,位于顶点和面心,若某一个P的坐标是(0,0,0),其余P的坐标可以是 (![]() ,
,![]() ,0)、(0,
,0)、(0,![]() ,
,![]() )、(
)、(![]() ,0,
,0,![]() )]等;B原子填入四面体空隙,且B的坐标是(
)]等;B原子填入四面体空隙,且B的坐标是(![]() ,
,![]() ,
,![]() )、(
)、(![]() ,
,![]() ,
,![]() )、(
)、(![]() ,
,![]() ,
,![]() )、(
)、(![]() ,
,![]() ,
,![]() ),磷化硼晶胞结构如图
),磷化硼晶胞结构如图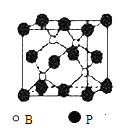 ,该晶体中每个B原子周围有12个B原子与它距离最近;相邻P原子和B原子最近的具有体对角线的1/4,则边长为
,该晶体中每个B原子周围有12个B原子与它距离最近;相邻P原子和B原子最近的具有体对角线的1/4,则边长为![]() cm,根据晶胞,推出磷化硼的化学式为BP,则晶胞的质量为
cm,根据晶胞,推出磷化硼的化学式为BP,则晶胞的质量为 ,根据密度的定义,该晶体的密度为
,根据密度的定义,该晶体的密度为![]() g/cm3。
g/cm3。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】三种难溶金属硫化物的溶度积常数(25℃):
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10﹣18 | 1.3×10﹣36 | 2.5×10﹣13 |
下列有关说法中正确的是( )
A.25℃时,CuS的溶解度大于MnS的溶解度
B.25℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10﹣36 molL﹣1
C.因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生
D.除去某溶液中的Cu2+ , 可以选用FeS作沉淀剂