题目内容
9.羧酸在自然界和日常生活中广泛存在,下列物质属于羧酸的是( )| A. | HCHO | B. | CH3CH2OH | C. | HCOOH | D. | HCOOCH3 |
分析 羧酸是羧基-COOH直接与链烃基或苯环相连的化合物,官能团为-COOH,据此分析.
解答 解:羧酸是羧基-COOH直接与链烃基或苯环相连的化合物,官能团为-COOH.
A、HCHO的官能团为醛基-CHO,属于醛类,故A错误;
B、CH3CH2OH的官能团为羟基-OH属于醇类,故B错误;
C、HCOOH的官能团为-COOH,属于酸类,故C正确;
D、HCOOCH3的官能团为酯基-COO-,属于酯类,故D错误.
故选C.
点评 本题考查了羧酸的官能团羧基,熟练掌握有机物的官能团是解题关键,难度不大.

练习册系列答案
相关题目
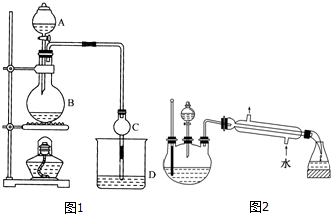
19.某课外小组设计的实验室制取乙酸乙酯的装置如图1所示,A中放有浓硫酸,B中放有乙醇(含180)、无水醋酸钠,D中放有含有酚酞饱和碳酸钠溶液.
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H50H
②有关有机物的沸点:
请回答:
(1)浓硫酸的作用是制乙酸、催化剂、吸水剂;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式:CH3COOH+CH3CH218OH CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.
(2)球形干燥管C的作用是防止倒吸、冷凝.反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(3)上述实验中饱和碳酸钠溶液的作用是中和乙酸并吸收乙醇,减少乙酸乙酯的溶解.
(4)欲从D中得到乙酸乙酯的分离方法是分液;从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇;
(5)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与图1装置相比,此装置的主要优点有:(请写出两点):①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的发生;②增加了冷凝装置,有利于收集产物乙酸乙酯.

已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H50H
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)浓硫酸的作用是制乙酸、催化剂、吸水剂;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式:CH3COOH+CH3CH218OH
 CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.(2)球形干燥管C的作用是防止倒吸、冷凝.反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(3)上述实验中饱和碳酸钠溶液的作用是中和乙酸并吸收乙醇,减少乙酸乙酯的溶解.
(4)欲从D中得到乙酸乙酯的分离方法是分液;从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇;
(5)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与图1装置相比,此装置的主要优点有:(请写出两点):①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的发生;②增加了冷凝装置,有利于收集产物乙酸乙酯.
20.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),在2L的密闭容器中进行,1min后,NH3减少0.12mol,则该反应的化学反应速率是( )
| A. | v(NH3)=0.002mol(L•s) | B. | v(H2O)=0.002mol/(L•s) | ||
| C. | v(NO)=0.0015mol/(L•s) | D. | v(O2)=0.00125mol/(L•s) |
17.下列关于实验室制备乙烯实验的说法中正确的是( )
| A. | 反应物是体积比1:3的乙醇和3mol/L硫酸的混和液 | |
| B. | 温度计插入反应溶液液面以下,以便控制反应温度 | |
| C. | 反应容器烧瓶中应加入少许瓷片 | |
| D. | 反应完毕先灭熄灭酒精灯,再从水槽中取出导管 |
4.下列溶液中微粒的关系不正确的是( )
| A. | 已知A-+H2B(过量)═HA+HB-,则结合H+的能力:HB-<A-<B2- | |
| B. | 常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性 | |
| C. | 浓度为0.1mol•L-1 的下列溶液,pH由大到小的排列顺序:NaOH>Na2CO3 >(NH4)2SO4 >NaHSO4 | |
| D. | 为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸,若pH<7,则H2A是强酸 |
14.下列有关说法正确的是( )
| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解 | |
| B. | Fe(OH)3胶体无色、透明,能产生丁达尔现象 | |
| C. | H2、SO2、CO2三种气体都可用浓H2SO4干燥 | |
| D. | SiO2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物 |
1.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 2L0.5mol/L亚硫酸溶液中含有的H+个数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
13.苯乙烯( )是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )
)是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )
 )是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )
)是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )| A. | 它能使溴的四氯化碳溶液褪色,但不能使酸性高锰酸钾溶液褪色 | |
| B. | 它既能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色 | |
| C. | 它易溶于水,也易溶于有机溶剂 | |
| D. | 在一定条件下可以发生加聚反应.生成物可用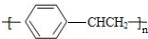 表示 表示 |
14.下列反应起了氮的固定作用的是( )
| A. | NH3经催化氧化获得NO | B. | NO2跟水作用制取硝酸 | ||
| C. | NH3+CO2+H2O=NH4HCO3 | D. | N2+O2=2NO(放电条件) |