题目内容
8.下列物质不能使潮湿的有色布条褪色的是( )| A. | 干燥的氯气 | B. | 久置的氯水 | C. | 液氯 | D. | 次氯酸溶液 |
分析 具有漂白性的物质有HClO、SO2、H2O2、O3等物质或能生成该物质的单质或化合物,由此分析解答.
解答 解:A、干燥的氯气不具有漂白性,则不能使干燥的有色布条褪色,但能与潮湿的有色布条中的水反应生成次氯酸,而使布条褪色,故A不选;
B、久置的氯水,是稀盐酸,不能使潮湿的有色布条褪色,故B选;
C、液氯能与潮湿的有色布条中的水反应生成次氯酸,而使布条褪色,故C不选;
D、次氯酸具有强氧化性,能使潮湿的有色布条褪色,故D不选;
故选B.
点评 本题考查氯气的性质及漂白性,为高频考点,把握干燥的氯气不具有漂白性,而潮湿的氯气具有漂白性为解答的关键,注意规律性知识的归纳,题目难度不大.

练习册系列答案
相关题目
18.下列电离方程式书写正确的是( )
| A. | KClO3═K++Cl5-+3O2- | B. | HNO3═H++NO3- | ||
| C. | Na2CO3═Na2++CO32- | D. | CaCl2═Ca2++Cl- |
19.分子式为C8H18的烃,其中主链上有6个碳原子的同分异构体有( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
16.下列各对物质中,互为同位素的是( )
①${\;}_{1}^{1}H$、${\;}_{1}^{2}H$ ②H2O、D2O ③${\;}_{17}^{35}Cl$、${\;}_{17}^{37}Cl$ ④金刚石、石墨 ⑤O2、O3⑥H2、H+.
①${\;}_{1}^{1}H$、${\;}_{1}^{2}H$ ②H2O、D2O ③${\;}_{17}^{35}Cl$、${\;}_{17}^{37}Cl$ ④金刚石、石墨 ⑤O2、O3⑥H2、H+.
| A. | ①②③ | B. | ①③ | C. | ③④⑤ | D. | ④⑤⑥ |
13. (1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.
(1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.
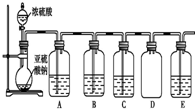
(2)该探究小组还根据SO2中S元素的化合价,预 测并通过实验探究SO2的其他性质.探究过程中选用的实验药品有:浓硫酸、亚硫酸钠固体、Na2S溶液、酸性高锰酸钾溶液、品红溶液等.探究过程的实验装置图如图所示,请回答下列问题.
①请你完成下列表格.
②A中发生反应的离子方程式为5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+.
③实验时C中的实验现象是品红溶液褪色.
④D装置的作用是防倒吸.E是尾气处理装置,有人认为E装置中可以加入足量的Ba(NO3)2溶液,你认为是否合理,请结合离子方程式加以说明:不合理,因为发生的反应为3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO↑+4H+,生成的NO仍然对环境有污染.
 (1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.
(1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.| 物质 | 类别 | 化学性 质预测 | 实验验证 | ||
| 实验操作 | 实验现象 | 实质(用离子 方程式表示) | |||
| 二氧 化硫 | 酸性 氧化物 | 与水 反应 | 将盛满SO2气体的试管倒立在水中,并测定试管中溶液的pH | ① | SO2+H2O ?H2SO3 |
| 与碱 反应 | ② | 出现白 色沉淀 | ③ | ||
①请你完成下列表格.
| 装置 | 药品 | 作用 |
| A | 验证二氧化硫的还原性 | |
| B | ||
| C | 品红溶液 |
③实验时C中的实验现象是品红溶液褪色.
④D装置的作用是防倒吸.E是尾气处理装置,有人认为E装置中可以加入足量的Ba(NO3)2溶液,你认为是否合理,请结合离子方程式加以说明:不合理,因为发生的反应为3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO↑+4H+,生成的NO仍然对环境有污染.
20.化学与生产、生活、社会密切相关,下列有关说法不正确的是( )
| A. | 利用ClO2对自来水消毒主要是因为ClO2具有强氧化性 | |
| B. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 | |
| C. | Al2O3的熔点很高,工业上用于制作耐高温材料,也用于冶炼铝 | |
| D. | 在食品袋中放入盛有硫酸亚铁的透气小袋,可防止食物受潮、氧化变质 |
17.合理用药,服务健康.下列对于常用药物知识的叙述正确的是( )
| A. | 阿司匹林具有解热镇痛、抗炎、抗风湿效用,可长期服用没有副作用 | |
| B. | 青霉素能有效治疗细菌引发的感染,而对病毒引起的疾病无治疗效果 | |
| C. | 治疗胃酸过多的药物中通常含有氢氧化铝、碳酸镁、碳酸氢钠等成分 | |
| D. | 对于标记“OTC”的药物,必需凭医师的处方才能购买 |