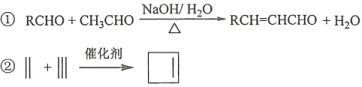
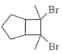
��Ŀ����
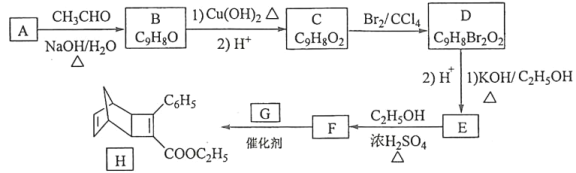
����Ŀ����֪A��һ�ֵ���ɫ���壬������������CΪ���д��Եĺ�ɫ���壬E����ɫ��ӦΪ��ɫ��FΪ���ɫ���壨���ֲ�������ȥ����
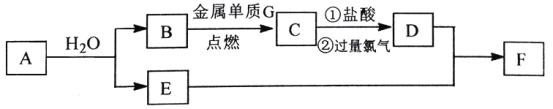
��1������A��F�Ļ�ѧʽ�ֱ���_____________��_____________��
��2��C��D�Ĺ����еڢڲ���Ӧ�����ӷ���ʽ��____________________________________��
��3����μ���D�еĽ��������ӣ�˵������IJ�����ʵ������________________________��
��4��E��Һ��ؿ��к������Ľ���Ԫ�صĵ��ʷ�����Ӧ�Ļ�ѧ����ʽΪ______________��
��5��G��D��ҺҲ�ܷ�����Ӧ���䷴Ӧ������Ϊ___________________������ţ���
a.���Ϸ�Ӧ b.�û���Ӧ c.���ֽⷴӦ d.������ԭ��Ӧ
���𰸡�Na2O2 Fe(OH)3 2Fe2+��Cl2=2Fe3+��2Cl�� ȡ����D��Һ���Թ��У��μ�KSCN��Һ����Һ��Ѫ��ɫ������������Ҳ�÷� 2Al��2NaOH��2H2O��2NaAlO2��3H2�� ad
��������
��֪A��һ�ֵ���ɫ���壬������������ӦΪNa2O2��CΪ���д��Եĺ�ɫ���壬ӦΪFe3O4��E����ɫ��ӦΪ��ɫ������ת����ϵ��֪EΪNaOH��BΪO2��DΪFeCl3��FΪ���ɫ���壬ӦΪFe(OH)3���Դ˽����⡣
��1�������Ϸ�����֪AΪNa2O2 ��FΪFe(OH)3 ���ʴ�Ϊ��Na2O2 �� Fe(OH)3 ��
��2��C��D�Ĺ����еڢڲ���Ӧ�����ӷ���ʽ��2Fe2++Cl2=2Fe3++2Cl-��
��3��DΪFeCl3��������Ϊ�����ӣ����������ӣ���ȡ����D��Һ���Թ��У��μ�KSCN��Һ���ɹ۲쵽��Һ��Ѫ��ɫ���ʴ�Ϊ��ȡ����D��Һ���Թ��У��μ�KSCN��Һ����Һ��Ѫ��ɫ��
��4���ؿ��к������Ľ���Ϊ�������������Ʒ�Ӧ�ķ���ʽΪ2Al+2NaOH+2H2O=2NaAlO2+3H2����
��5�������Ȼ�����Ӧ�����Ȼ�������Ϊ���Ϸ�Ӧ��������ԭ��Ӧ���ʴ�Ϊ��ad��