题目内容
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+的电子排布式为_________________。
(2)实验室用KSCN溶液、苯酚(![]() )检验Fe3+。N、O、S的第一电离能由大到小的顺序为______(用元素符号表示),苯酚中碳原子的杂化轨道类型为_______。
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为______(用元素符号表示),苯酚中碳原子的杂化轨道类型为_______。
(3)FeCl3的熔点为306℃,沸点为315℃。FeCl3的晶体类型是________。FeSO4常作补铁剂,SO42-的立体构型是__________。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。1 mol Fe(CO)5分子中含________molσ键,与CO互为等电子体的离子是__________(填化学式,写一种)。
(5)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为_____。

(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-的最短核间距为___________pm。
【答案】1s22s22p63s23p63d5或[Ar]3d5 N>O>S sp2 分子晶体 正四面体形 10 CN-或C22- 3:1 12 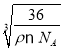 ×1010
×1010
【解析】
(1)铁为26号元素,电子排布式为1s22s22p63s23p63d64s2,失去4s能级上的2个电子,形成Fe2+,再失去3d能级上的1个电子后形成Fe3+;
(2)同周期从左向右第一电离能逐渐增大,同主族从上到下第一电离能逐渐减小;苯酚可看成分子中的一个氢原子被羟基取代,苯和苯酚均为平面结构,碳原子均为sp2杂化;
(3)分子晶体熔沸点较低且熔融状态不导电;根据SO42-中心原子含有的共价键个数与孤电子对数之和确定空间构型;
(4)配合物中碳原子不存在孤电子对,σ键由2个,即1个Fe(CO)5中含有10个σ键;原子数目相等,价电子总数相等的微粒为等电子体;
(5)氮化铁晶体为六棱柱,顶点为6个晶胞共有,面心的点为2个晶胞共有,晶胞中12个铁原子位于顶点,2个铁原子位于面心,3个铁原子位于内部,2个氮原子位于内部,因此据此可计算微粒个数比;
(6)以Fe2+顶点研究,与Fe2+紧邻且等距离的Fe2+处于面心,每个顶点为8个晶胞共用,每个面为2个晶胞共用;Fe2+与O2-的最短核间距等于晶胞棱长的![]() ,均摊法计算晶胞中Fe2+与O2-的离子数目,计算出晶胞的质量,与密度公式结合进行计算。
,均摊法计算晶胞中Fe2+与O2-的离子数目,计算出晶胞的质量,与密度公式结合进行计算。
(1)铁原子失去4s能级上的2个电子和3d能级上的1个电子后形成Fe3+,因此基态Fe3+的电子排布式为1s22s22p63s23p63d5或[Ar]3d5;
(2)同主族从上到下第一电离能逐渐减小,即第一电离能O>S,同周期从左向右第一电离能逐渐增大,但氮元素2p能级处于半满的稳定状态,能量低,因此第一电离能N>O,所以第一电离能N>O>S;苯酚可看成分子中的一个氢原子被羟基取代,苯和苯酚均为平面结构,碳原子均为sp2杂化
(3)FeCl3的熔点为306℃,沸点为315℃,熔沸点较低,属于分子晶体;SO42-中心S原子的σ键电子对数为4,中心原子孤电子对数为0,价层电子对数为4,立体构型为正四面体形;
(4)配合物中碳原子不存在孤电子对,σ键由2个,即1个Fe(CO)5中含有10个σ键,那么1 mol Fe(CO)5分子中含10molσ键;原子数目相等,价电子总数相等的微粒为等电子体,与CO互为等电子体的离子有CN-或者C22-;
(5)氮化铁晶体为六棱柱,顶点为6个晶胞共有,面心的点为2个晶胞共有,晶胞中12个铁原子位于顶点,2个铁原子位于面心,3个铁原子位于内部,2个氮原子位于内部,因此晶胞中含有铁微粒12×![]() +2×
+2×![]() +3=6,氮微粒的个数为2,所以铁、氮的微粒个数之比为6:2=3:1;
+3=6,氮微粒的个数为2,所以铁、氮的微粒个数之比为6:2=3:1;
(6)以Fe2+顶点研究,与Fe2+紧邻且等距离的Fe2+处于面心,每个顶点为8个晶胞共用,每个面为2个晶胞共用,因此与Fe2+紧邻且等距离的Fe2+数目为![]() =12个;晶胞中Fe2+共8×
=12个;晶胞中Fe2+共8×![]() +6×
+6×![]() =4,O2-的数目为1+12×
=4,O2-的数目为1+12×![]() =4,晶胞的质量为
=4,晶胞的质量为![]() ,Fe2+与O2-的最短核间距等于晶胞棱长的
,Fe2+与O2-的最短核间距等于晶胞棱长的![]() ,设最短距离为xpm,则晶胞的棱长为2xpm,那么
,设最短距离为xpm,则晶胞的棱长为2xpm,那么![]() =ρ(2x×10-10)3,解得x=
=ρ(2x×10-10)3,解得x=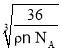 ×1010pm。
×1010pm。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案